摘要:20080916 10.用NA表示阿佛加德罗常数.下列叙述正确的是 ( ) A.一定温度.压强下.气体体积由其分子的大小决定 B.46gNO2和N2O4的混合物中含有的原子总数一定是3NA个 C.在标准状况下.含NA个氦原子(He)的氦气所含的分子数是0.5NA D.25℃时.1 L pH=13的氢氧化钠溶液中含有NA个氢氧根离子11.下列反应的离子方程式书写正确的是 ( ) A.小苏打溶液和甲酸溶液混合 HCO3-+HCOOH=HCOO-+CO2↑+H2O B.铝片放入NaOH溶液中 2OH-+Al=AlO2-+H2↑ C.次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO D.氨水中通入少量二氧化硫 2NH3·H2O+SO2=2NH4++SO32-+H2O
网址:http://m.1010jiajiao.com/timu_id_1735363[举报]
下列说法正确的数目为( )
①硫酸铜可作为过氧化氢分解反应的催化剂
②向重铬酸钾溶液中加入烧碱溶液会使溶液逐渐变为绿色
③向氯化铁溶液中滴加硫氰酸钾溶液会产生血红色沉淀
④物质的量相同的磷酸钠溶液和磷酸溶液中所含磷酸根的量相同
⑤充电电池的记忆效是由于不当的充放电方式造成的
⑥水的电离平衡常数,即水的离子积KW,在100°C时数值为55×10-14
⑦用含氟牙膏刷牙可以防龋齿是因为氟离子会抑制牙的溶解
⑧明矾的水溶液蒸干会得到硫酸铝.
①硫酸铜可作为过氧化氢分解反应的催化剂
②向重铬酸钾溶液中加入烧碱溶液会使溶液逐渐变为绿色
③向氯化铁溶液中滴加硫氰酸钾溶液会产生血红色沉淀
④物质的量相同的磷酸钠溶液和磷酸溶液中所含磷酸根的量相同
⑤充电电池的记忆效是由于不当的充放电方式造成的
⑥水的电离平衡常数,即水的离子积KW,在100°C时数值为55×10-14
⑦用含氟牙膏刷牙可以防龋齿是因为氟离子会抑制牙的溶解
⑧明矾的水溶液蒸干会得到硫酸铝.
| A、2 | B、3 | C、4 | D、5 |
下列变化中涉及化学变化的是( )
(1)爆竹燃放(2)碘的升华(3)金属钝化(4)铝热反应(5)橡胶老化(6)甘油加水作护肤剂(7)蜂蚁蛰咬皮肤后涂稀氨水(8)医用酒精可用于皮肤消毒(9)烹鱼时加入少量的料酒和食醋(10)用四氯化碳可擦去圆珠笔油渍.
(1)爆竹燃放(2)碘的升华(3)金属钝化(4)铝热反应(5)橡胶老化(6)甘油加水作护肤剂(7)蜂蚁蛰咬皮肤后涂稀氨水(8)医用酒精可用于皮肤消毒(9)烹鱼时加入少量的料酒和食醋(10)用四氯化碳可擦去圆珠笔油渍.
查看习题详情和答案>>
实验:
(1)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: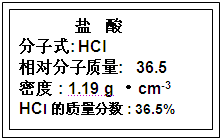
①该浓盐酸中HCl的物质的量浓度为
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D溶液的密度
(2)实验室配制480mL0.08mol/LNa2CO3溶液回答下列问题
①应用托盘天平称取十水碳酸钠晶体
②若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则实际称量的碳酸钠晶体是
③用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
A、干燥的 B、瓶塞不漏水 C、用欲配制的溶液润洗过 D、以上三项都要求
④若实验遇下列情况,溶液的浓度是“偏高”、“偏低”还是“不变”?
A.加水时越过刻度线
B.忘记将洗涤液加入容量瓶
C.容量瓶内壁附有水珠而未干燥处理
D.溶解后没有冷却便进行定容
(3)①取少量Fe2O3粉末(红棕色)加入适量盐酸,反应的离子方程式为
②取少量溶液置于试管中,滴入NaOH溶液,看到有红褐色沉淀生成,反应的离子方程式为
③在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL FeCl3饱和溶液,继续煮沸至溶液呈
④另取一小烧杯加入25mL蒸馏水后,向烧杯中再加入2mL FeCl3饱和溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到
查看习题详情和答案>>
(1)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

①该浓盐酸中HCl的物质的量浓度为
11.9
11.9
mol?L-1.②取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是BD
BD
.A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D溶液的密度
(2)实验室配制480mL0.08mol/LNa2CO3溶液回答下列问题
①应用托盘天平称取十水碳酸钠晶体
11.4
11.4
g②若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则实际称量的碳酸钠晶体是
10.6
10.6
g(1g以下用游码)③用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
B
B
A、干燥的 B、瓶塞不漏水 C、用欲配制的溶液润洗过 D、以上三项都要求
④若实验遇下列情况,溶液的浓度是“偏高”、“偏低”还是“不变”?
A.加水时越过刻度线
偏低
偏低
;B.忘记将洗涤液加入容量瓶
偏低
偏低
;C.容量瓶内壁附有水珠而未干燥处理
不变
不变
;D.溶解后没有冷却便进行定容
偏高
偏高
.(3)①取少量Fe2O3粉末(红棕色)加入适量盐酸,反应的离子方程式为
Fe2O3+6H+=2Fe3++3H2O
Fe2O3+6H+=2Fe3++3H2O
,反应后得到黄色的FeCl3溶液.用此溶液做以下实验:②取少量溶液置于试管中,滴入NaOH溶液,看到有红褐色沉淀生成,反应的离子方程式为
Fe3++3O H-=Fe(OH)3↓
Fe3++3O H-=Fe(OH)3↓
.③在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL FeCl3饱和溶液,继续煮沸至溶液呈
红褐
红褐
色,即可制得Fe(OH)3胶体.④另取一小烧杯加入25mL蒸馏水后,向烧杯中再加入2mL FeCl3饱和溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到
乙
乙
(填甲或乙)烧杯中会产生丁达尔效应.此实验可以区别溶液和胶体
溶液和胶体
. 已知E与G反应生成L和M,且组成E、G、L、M分子的元素原子序数均小于10,用它们的结构式表示反应如图所示.则下列判断错误的是( )
已知E与G反应生成L和M,且组成E、G、L、M分子的元素原子序数均小于10,用它们的结构式表示反应如图所示.则下列判断错误的是( )