摘要:31.[化学-化学与技术] 现代社会中铜在电气.交通.机械和冶金.能源及石化工业.高科技等领域有广泛的应用.某铜矿石含氧化铜.氧化亚铜.三氧化二铁和脉石(SiO2).现采用酸浸法从矿石中提取铜.其工艺流程图如下.其中铜的萃取(铜从水层进入有机层的过程)和反萃取(铜从有机层进入水层的过程)是现代湿法炼铜的重要工艺手段. 已知:①Cu+在酸性溶液中不稳定.可发生自身氧化还原反应,②当矿石中三氧化二铁含量太低时.可用硫酸和硫酸铁的混合液浸出铜,③反萃取后的水层2是硫酸铜溶液. 回答下列问题: (1)矿石用稀硫酸处理过程中Cu2O发生反应的离子方程式为: , (2)“循环I 经多次循环后的水层1不能继续循环使用.但可分离出一种重要的硫酸盐晶体.该晶体的化学式是 .若水层1暴露在空气中一段时间后.可以得到另一种重要的硫酸盐.写出水层1暴露在空气中发生反应的离子方程式 . (3)写出电解过程中阳极发生反应的电极反应式: . (4)“循环III 中反萃取剂的主要成分是 .
网址:http://m.1010jiajiao.com/timu_id_1734412[举报]
[化学一选修化学与技术]
现代化工厂的设计理念是依据循环经济理论和工业生态学原理建立生态工业园区.如图是某企业设计的硫酸一磷铵一水泥联产、海水-淡水多用、盐一热一电联产的三大生态产业链流程图.

根据上述产业流程回答下列问题:
(1)从原料、能源、交通角度考虑该企业应建在
A西部山区 B沿海地区 C发达城市 D东北内陆
(2)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:① 、② 、③ 、④ 、⑤ .
(3)沸腾炉发生反应的化学方程式: ;磷肥厂的主要产品是普钙,其主要成分是 (填化学式).
(4)热电厂的冷却水是 ,该流程中浓缩盐水除提取盐以外还可提取的物质有 (写出一种即可).
(5)根据现代化工厂没计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想. , (写出两点即可).
查看习题详情和答案>>
现代化工厂的设计理念是依据循环经济理论和工业生态学原理建立生态工业园区.如图是某企业设计的硫酸一磷铵一水泥联产、海水-淡水多用、盐一热一电联产的三大生态产业链流程图.

根据上述产业流程回答下列问题:
(1)从原料、能源、交通角度考虑该企业应建在
A西部山区 B沿海地区 C发达城市 D东北内陆
(2)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:①
(3)沸腾炉发生反应的化学方程式:
(4)热电厂的冷却水是
(5)根据现代化工厂没计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想.
合成氨是人类科学技术上的一项重大突破,是化学与技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸)为:Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac 请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为________。
(2)写出基态Cu+的核外电子排布式:___________。
(3)配合物Cu(NH3)3(CO)Ac的中心离子的配位数为________。
(4)写出与CO互为等电子体的离子__________(任写一个)。
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中C原子的轨道杂化类型是________;1 mol尿素分子中,σ键的数目为____。
(6)铜金合金形成的晶胞如下图所示,其中Cu、Au原子个数比为___________。
(1)C、N、O的第一电离能由大到小的顺序为________。
(2)写出基态Cu+的核外电子排布式:___________。
(3)配合物Cu(NH3)3(CO)Ac的中心离子的配位数为________。
(4)写出与CO互为等电子体的离子__________(任写一个)。
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中C原子的轨道杂化类型是________;1 mol尿素分子中,σ键的数目为____。
(6)铜金合金形成的晶胞如下图所示,其中Cu、Au原子个数比为___________。

【化学-选修化学与技术】
海水中镁的总储量约为2.1×1015 t,目前世界生产的镁60%来自海水.海水的综合利用可以制备金属镁,其流程如下图所示:

其步骤为:
①将海边大量存在的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
②将石灰乳加入到经过蒸发浓缩并滤去粗盐后的海水中,过滤得到Mg(OH)2沉淀;
③向Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O;
④将MgCl2?6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的MgCl2可得到Mg.
请回答下列问题:
(1)步骤①中煅烧贝壳时所发生反应的化学方程式为 .
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为 .
(3)步骤③中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有 、 、酒精灯、铁架台等.
(4)海水中的镁以Mg2+的形式存在,设计步骤②③将Mg2+转化为Mg(OH)2,然后又重新转化为Mg2+的目的是 .
(5)步骤④中的“一定条件”指的是 ,目的是 .
(6)在上述制取镁的流程中,所涉及到的基本反应类型有 .
a.化和反应b.分解反应c.置换反应d.复分解反应
(7)由海水得到的粗盐中常含有Ca2+、Mg2+、SO42-等杂质,为除去这些杂质可加入Na2CO3、NaOH和BaCl2,然后过滤,则所加入试剂的合理顺序为 .
查看习题详情和答案>>
海水中镁的总储量约为2.1×1015 t,目前世界生产的镁60%来自海水.海水的综合利用可以制备金属镁,其流程如下图所示:

其步骤为:
①将海边大量存在的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
②将石灰乳加入到经过蒸发浓缩并滤去粗盐后的海水中,过滤得到Mg(OH)2沉淀;
③向Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O;
④将MgCl2?6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的MgCl2可得到Mg.
请回答下列问题:
(1)步骤①中煅烧贝壳时所发生反应的化学方程式为
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为
(3)步骤③中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有
(4)海水中的镁以Mg2+的形式存在,设计步骤②③将Mg2+转化为Mg(OH)2,然后又重新转化为Mg2+的目的是
(5)步骤④中的“一定条件”指的是
(6)在上述制取镁的流程中,所涉及到的基本反应类型有
a.化和反应b.分解反应c.置换反应d.复分解反应
(7)由海水得到的粗盐中常含有Ca2+、Mg2+、SO42-等杂质,为除去这些杂质可加入Na2CO3、NaOH和BaCl2,然后过滤,则所加入试剂的合理顺序为
(2011?沈阳二模)化学----化学与技术模块
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
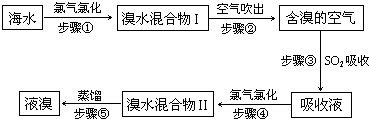
(1)步骤①反应的离子方程式是
(2)步骤③反应的化学方程式是
(3)Br的原子序数是
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃.温度过高或过低都不利于生产,请解释原因:
(5)为什么不直接用“溴水混合物I”而要用“溴水混合物II”进行蒸馏,得到液溴?
查看习题详情和答案>>
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:

(1)步骤①反应的离子方程式是
2Br-+Cl2=2Cl-+Br2
2Br-+Cl2=2Cl-+Br2
.(2)步骤③反应的化学方程式是
SO2+Br2+2H2O=2HBr+H2SO4
SO2+Br2+2H2O=2HBr+H2SO4
.(3)Br的原子序数是
35
35
,在周期表中位于4
4
周期ⅤⅡA
ⅤⅡA
族.(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃.温度过高或过低都不利于生产,请解释原因:
温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低
温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低
.(5)为什么不直接用“溴水混合物I”而要用“溴水混合物II”进行蒸馏,得到液溴?
溴水混合物I成分复杂,要获得溴需控制多个温度,操作麻烦
溴水混合物I成分复杂,要获得溴需控制多个温度,操作麻烦
.(化学--选修化学与技术)
海水中溶解了大量的气体物质和各种盐类.人类在陆地上发现的100多种元素,在海水中可以找到80多种.海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景.回答下列问题:
(1)蒸馏法是人类最早使用的淡化海水的方法,技术和工艺比较完备,但由于使用大量燃煤,因此能耗多、排污量大.为克服蒸馏法海水淡化的缺陷,请你对蒸馏法淡化海水的工艺提出一条改进建议
(2)使用离子交换树脂与水中的离子进行交换也是常用的水处理技术.聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
(3)空气吹出法是目前从海水中提取溴的常用方法,流程如下(苦卤:海水蒸发结晶分离出食盐后的母液):
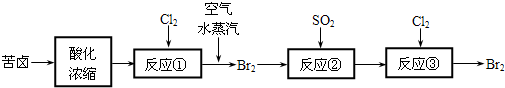
①反应②的离子方程式为
(4)苦卤中含有NaCl、MgCl2、KCl、MgSO4.用简要的文字说明如何测定苦卤中MgCl2的含量
查看习题详情和答案>>
海水中溶解了大量的气体物质和各种盐类.人类在陆地上发现的100多种元素,在海水中可以找到80多种.海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景.回答下列问题:
(1)蒸馏法是人类最早使用的淡化海水的方法,技术和工艺比较完备,但由于使用大量燃煤,因此能耗多、排污量大.为克服蒸馏法海水淡化的缺陷,请你对蒸馏法淡化海水的工艺提出一条改进建议
充分利用潮汐能、风能、太阳能等海边富有的洁净能源
充分利用潮汐能、风能、太阳能等海边富有的洁净能源
.(2)使用离子交换树脂与水中的离子进行交换也是常用的水处理技术.聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
CH2=CHCOONa
CH2=CHCOONa
.(3)空气吹出法是目前从海水中提取溴的常用方法,流程如下(苦卤:海水蒸发结晶分离出食盐后的母液):

①反应②的离子方程式为
SO2+Br2+2H2O=4H++2Br-+SO42-
SO2+Br2+2H2O=4H++2Br-+SO42-
; ②从反应③后的四氯化碳溶液中分离出单质溴的方法是蒸馏
蒸馏
.(4)苦卤中含有NaCl、MgCl2、KCl、MgSO4.用简要的文字说明如何测定苦卤中MgCl2的含量
先用足量BaCl2溶液沉淀硫酸根离子,求出硫酸根离子的总量,并求出MgSO4的量,然后用足量NaOH溶液沉淀Mg2+,求出总的Mg2+,减去MgSO4中的Mg2+得到MgCl2的量
先用足量BaCl2溶液沉淀硫酸根离子,求出硫酸根离子的总量,并求出MgSO4的量,然后用足量NaOH溶液沉淀Mg2+,求出总的Mg2+,减去MgSO4中的Mg2+得到MgCl2的量
.