摘要:26.将3.20g Cu溶于B mol/L过量的硝酸溶液30.0 mL中.假设硝酸的还原产物只有NO2和NO.反应结束后.将所剩余溶液加水稀释至1000 mL.测得. (1)试求稀释后溶液的pH. (2)求生成的气体中NO2和NO的物质的量(可以含有B的代数式表示). (3)用NaOH溶液吸收氮的氧化物是防止污染的一种方法.原理为: . 若生成的混合气体能被NaOH溶液完全吸收.试讨论B的取值范围.
网址:http://m.1010jiajiao.com/timu_id_1734250[举报]
将3.20 g Cu溶于B mol·L-1过量的硝酸溶液30.0 mL中,假设硝酸的还原产物只有NO2和NO,反应结束后,将所剩溶液加水稀释至1 000 mL,测得c( )=0.200 mol·L-1。
)=0.200 mol·L-1。
(1)试求稀释后溶液的pH。
(2)生成的气体中NO2和NO的物质的量 (可用含有B的代数式表示)。
(3)用NaOH溶液吸收氮的氧化物是防止NOx污染的一种方法。原理为:2NO2+2NaOH====NaNO3+NaNO2+H2O,NO+NO2+2NaOH====2NaNO2+H2O
若生成的混合气体能被NaOH溶液完全吸收,试讨论B的取值范围。
查看习题详情和答案>>
将3.2 g Cu溶于B mol·L -1过量的硝酸溶液30.00 mL中,假设硝酸的还原产物只有NO2和NO。反应结束后,将所得剩余溶液加水稀释至1000 mL,测得c(NO3 -)=0.200 mol·L-1。
(1)求稀释后溶液的pH(要求写出计算过程)。
(2)生成的气体中NO2的物质的量(用含有B的表达式表示)
n(NO2)=_________________mol。
查看习题详情和答案>> [化学--物质结构与性质
[化学--物质结构与性质 Ⅰ.(1)原子数相同,价电子数也相同的微粒,称为等电子体.等电子体具有相似的化学键特征,性质相似.CO的结构式为
C≡O
C≡O
.Ⅱ.(2)钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、航天航空材料,被誉为“未来世界的金属”. 钛的基态原子的电子排布式为
1s22s22p63s23p63d24s2
1s22s22p63s23p63d24s2
.(3)偏钛酸钡在小型变压器、话筒和扩音器中都有●Ti应用.偏钛酸钡为离子晶体,晶胞的结构如图 所示,它的化学式是
BaTiO3
BaTiO3
.(4)现有含Ti3+的配合物,化学式为TiCl3(H2O)6,将1mol该物质溶于水,加入足量硝酸银溶液,立即沉淀的氯化银为l mol,已知该配合物的配位数为6,则该配合物的配位体是
Cl-、H2O
Cl-、H2O
.1mol该配合物外界所含 结晶水的物质的量为2
2
mol.(8分)、钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
(1)钛有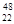 Ti和
Ti和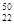 Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 周期,第 族;按电子排布Ti元素在元素周期表分区中属于 (填s、p、d、ds或f)区元素
Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 周期,第 族;按电子排布Ti元素在元素周期表分区中属于 (填s、p、d、ds或f)区元素
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛酸钡为离子晶体,晶胞的结构如右图所示,它的化学式是 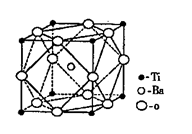
(3)现有含Ti3+的配合物,化学式为TiCl3(H2O)6,将1mol该物质溶于水,加入足量硝酸银溶液,立即沉淀的氯化银为1mol,已知该配合物的配位数为6,则该配合物的配位体是 。
1mol该配合物外界所含结晶水物质的量为 mol。