摘要:请写出下列①~⑥步的转化中所发生的化学反应方程式.并注明化学反应类型. ① 反应类型 ② 反应类型 ③ 反应类型 ④ 反应类型 ⑤ 反应类型 ⑥ 反应类型
网址:http://m.1010jiajiao.com/timu_id_1733854[举报]
某化学兴趣小组测定某FeCl3样品(含有少量FeCl2杂质)中铁元素的质量分数,实验时按以下步骤进行:
①称量ag样品,置于烧杯中,
②加入适量的蒸馏水,使样品溶解,然后准确配制成250mL溶液
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀声称到坩埚内加热,搅拌直到固体全部由红褐色变为红棕色后在干燥器中冷却到室温后,称量
⑦…根据上面叙述,回答
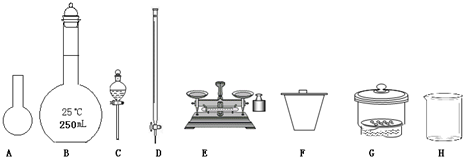
(1)如图所示仪器中,本实验步骤①②中必须用到的仪器是
(2)写出步骤③和④中发生反应的离子方程式
(3)洗涤是洗去附着在沉淀上的
(4)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为
×100%
×100%(列出算式,不需化简)
(5)该兴趣小组中甲学生认为:实验步骤中不加氨水,其余步骤不变,仍可达到实验目的,你认为甲学的观点是否正确
查看习题详情和答案>>
①称量ag样品,置于烧杯中,
②加入适量的蒸馏水,使样品溶解,然后准确配制成250mL溶液
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀声称到坩埚内加热,搅拌直到固体全部由红褐色变为红棕色后在干燥器中冷却到室温后,称量
⑦…根据上面叙述,回答
(1)如图所示仪器中,本实验步骤①②中必须用到的仪器是
BE
BE
.
(2)写出步骤③和④中发生反应的离子方程式
2Fe2++Cl2=2Fe3++2Cl-;Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
2Fe2++Cl2=2Fe3++2Cl-;Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
(3)洗涤是洗去附着在沉淀上的
NH4+、Cl-、OH-
NH4+、Cl-、OH-
(写离子符号).洗涤沉淀的操作是向过滤器中加入蒸馏水至没过沉淀,待滤液流出后重复上述操作多次直至洗净为止
向过滤器中加入蒸馏水至没过沉淀,待滤液流出后重复上述操作多次直至洗净为止
检验沉淀已洗净的方法是取最次一次洗出液置于小试管中,滴加AgNO3溶液若无沉淀产生证明已洗净
取最次一次洗出液置于小试管中,滴加AgNO3溶液若无沉淀产生证明已洗净
(4)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为
| (w2-w1)×112×10 |
| 160a |
| (w2-w1)×112×10 |
| 160a |
(5)该兴趣小组中甲学生认为:实验步骤中不加氨水,其余步骤不变,仍可达到实验目的,你认为甲学的观点是否正确
正确
正确
(填“正确”或“错误”)请说明理由(必要时可用化学方程式表示)氯化铁溶液中Fe3+水解Fe3++3H2O?Fe(OH)3+3H+,加热HCl挥发,促进水解进行,过一系列转化最终都能生成Fe2O3对后续实验无影响
氯化铁溶液中Fe3+水解Fe3++3H2O?Fe(OH)3+3H+,加热HCl挥发,促进水解进行,过一系列转化最终都能生成Fe2O3对后续实验无影响
.【化学——选修:有机化学基础】( 15分)
通常羟基与烯键碳原子相连接时,易发生如下转化:
现有如图所示的转化关系:

其中E能使FeCl3溶液显紫色,遇Na2CO3溶液产生CO2气体,且测出E的核磁共振氢谱有4个峰,其面积之比为1:2 : 2 :1。
请根据以上信息回答下列问题:
(1)A的结构简式为 ;
(2)由A生成C和D的化学方程式为 ;
(3)由E生成C7H5O3Na的化学反应方程式为 ;
(4)若由E反应生成 ,则中间共需经历 步反应才能实现(除最后一步酸化外);
,则中间共需经历 步反应才能实现(除最后一步酸化外);
(5)请写出同时符合下列要求的E的所有同分异构体的结构简式:
。
①含苯环 ②苯环上一氯代物有两种 ③能发生银镜反应,不能发生水解反应
某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验时按以下步骤进行:
①称量a g样品,置于烧杯中
②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250 mL溶液
③准确量取25.00 mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀转移到某容器中,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量
⑦……
请根据上面叙述,回答:
(1)如图所示仪器中,本实验步骤①②③中必须用到的仪器是E和________(填字母)。
①称量a g样品,置于烧杯中
②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250 mL溶液
③准确量取25.00 mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀转移到某容器中,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量
⑦……
请根据上面叙述,回答:
(1)如图所示仪器中,本实验步骤①②③中必须用到的仪器是E和________(填字母)。

(2)步骤②中加入盐酸的作用_______________。
(3)写出步骤④中发生反应的离子方程式_________________。
(4)步骤③中加入适量氯水的目的__________ 样品中的杂质Fe2+有较强的还原性,氯水可改为NaClO3,完成并配平下列反应的离子方程式:___Fe2+ +___ClO3-+____=____Fe3+ +____Cl-+ ____H2O
(5)第⑥步的操作中,将沉淀物转移到___(填仪器名称)中灼烧,冷却至室温,称量其质量为m1g,再次加热并冷却至室温称量其质量为m2 g,若m1与m2 差值较大,接下来的操作应当是_________ 。
查看习题详情和答案>>
(3)写出步骤④中发生反应的离子方程式_________________。
(4)步骤③中加入适量氯水的目的__________ 样品中的杂质Fe2+有较强的还原性,氯水可改为NaClO3,完成并配平下列反应的离子方程式:___Fe2+ +___ClO3-+____=____Fe3+ +____Cl-+ ____H2O
(5)第⑥步的操作中,将沉淀物转移到___(填仪器名称)中灼烧,冷却至室温,称量其质量为m1g,再次加热并冷却至室温称量其质量为m2 g,若m1与m2 差值较大,接下来的操作应当是_________ 。
某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验时按以下步骤进行:
①称量a g样品,置于烧杯中
②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250 mL溶液
③准确量取25.00 mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀转移到坩埚内,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量
⑦……
请根据上面叙述,回答:
(1)如图所示仪器中,本实验步骤①②③中必须用到的仪器是E和________(填字母)。
①称量a g样品,置于烧杯中
②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250 mL溶液
③准确量取25.00 mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀转移到坩埚内,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量
⑦……
请根据上面叙述,回答:
(1)如图所示仪器中,本实验步骤①②③中必须用到的仪器是E和________(填字母)。

(2)写出步骤③中发生反应的离子方程式________。
(3)洗涤是洗去附着在沉淀上的________(写离子符号),洗涤沉淀的操作是______________。
(4)第⑥步的操作中,将沉淀物加热,冷却至室温,称量其质量为m1 g;再次加热并冷却至室温称量其质量为m2 g,且m1-m2=0.3,接下来的操作应当是______________________。
(5)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为_______。 (列出算式,不需化简)
(6)该兴趣小组中甲学生认为:实验步骤③中不加入氯水,其余步骤不变,仍可达到实验目的。你认为甲学生的观点是否正确?________(填“正确”或“错误”),请说明理由:________________。
查看习题详情和答案>>
(3)洗涤是洗去附着在沉淀上的________(写离子符号),洗涤沉淀的操作是______________。
(4)第⑥步的操作中,将沉淀物加热,冷却至室温,称量其质量为m1 g;再次加热并冷却至室温称量其质量为m2 g,且m1-m2=0.3,接下来的操作应当是______________________。
(5)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为_______。 (列出算式,不需化简)
(6)该兴趣小组中甲学生认为:实验步骤③中不加入氯水,其余步骤不变,仍可达到实验目的。你认为甲学生的观点是否正确?________(填“正确”或“错误”),请说明理由:________________。
