摘要:13.2L K2SO4 与CuSO4的混合溶液中.c(SO42-)=2mol/L.用石墨做电极电解此溶液.当通电一段时间后.两极均收集到22.4L气体.原溶液中c(K+)为 ( ) A.1.5mol/L B.2 mol/L C.3mol/L D.6mol/L 20080419 第Ⅱ卷
网址:http://m.1010jiajiao.com/timu_id_1733011[举报]
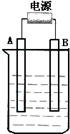 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:(1)请写出B极板的名称及反应式:
(2)写出电解时反应的总离子方程式
(3)若当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.电解后溶液的pH为
(4)若原溶液为1L K2SO4、CuSO4的混合溶液,且c(SO42-)=2.0mol/L;如图装置电解,当两极都收集到22.4L气体(标准状况)时,停止电解.则原溶液中的c(K+)为多少?(请简单表示计算过程)
(2013?鹿城区模拟)用石墨电极电解100mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
查看习题详情和答案>>
 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色硫酸盐溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色硫酸盐溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:(1)请写出B极板的名称:
阳极
阳极
电极反应式4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
写出电解时反应的总离子方程式
2Cu2++2H2O
2Cu+O2↑+4H+
| ||
2Cu2++2H2O
2Cu+O2↑+4H+
| ||
(2)若当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.电解后溶液的pH为
PH=1
PH=1
;要使电解后溶液恢复到电解前的状态,则需加入CuO
CuO
,其质量为2
2
g.(假设电解前后溶液的体积不变)(3)若原溶液为1L K2SO4、CuSO4的混合溶液,且c(SO42-)=2.0mol/L;如图装置电解,当两极都收集到22.4L气体(标准状况)时,停止电解.则原溶液中的c(K+)=
2mol/L
2mol/L
.