网址:http://m.1010jiajiao.com/timu_id_1732931[举报]
二茂铁(C5H5)2Fe是由一个二价铁离子和2个环戊烯基负离子构成,它的发现可以说是有机金属化合物研究中具有里程碑意义的事件,它开辟了金属有机化合物研究的新领域,促进了金属有机化学的发展.二茂铁可以用还原铁粉与环戊二烯在氮气氛围中发生反应而制得:2C5H6+Fe(还原铁粉)
| 300℃ | K2O.N2 |
请回答下列问题:
(1)写出二价铁离子的基态电子排布式:
(2)二茂铁的熔点是173℃(在100℃时开始升华),沸点是249℃,不溶于水,易溶于苯、乙醚等非极性溶剂.据此可推断二茂铁晶体为
(3)环戊二烯的结构式为:
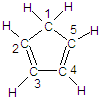 (图中数字仅代表碳原子编号),在其5个碳原子中采取sp3杂化的是
(图中数字仅代表碳原子编号),在其5个碳原子中采取sp3杂化的是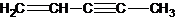 是环茂二烯的一种同分异构体,在其分子结构中处于同一平面上的原子个数最多有
是环茂二烯的一种同分异构体,在其分子结构中处于同一平面上的原子个数最多有(4)原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征.与N2分子互为等电子体的二价阴离子是
请回答下列问题:
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
| 电离能 I1 I2 I3 I4 … |
| In/kJ.mol-1 578 1817 2745 11578 … |
(2)基态锗(Ge)原子的电子排布式是
A.是一种活泼的金属元素 B.其电负性大于硫 C.其单质可作为半导体材料 D.其最高价氯化物的沸点低于其溴化物的沸点
(3)关于化合物
 ,下列叙述正确的有
,下列叙述正确的有A.分子间可形成氢键 B.分子中既有极性键又有非极性键 C.分子中有7个σ键和1个π键 D.该分子在水中的溶解度大于2-丁烯
(4)NaF的熔点
 的熔点(填>、=或<),其原因是
的熔点(填>、=或<),其原因是(A)“物质结构与性质”课程模块
下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于ds区的元素是___________ (填编号)。
(2)表中元素①的2个原子与元素③的2个原子形成的分子中元素③的杂化类型是________;③和⑦形成的常见化合物的化学键类型是___________。
(3)元素⑧的外围电子排布式为___________,该元素原子中未成对电子数为___________。
(4)在周期表中位于对角线的元素的性质也有一定的相似性。试写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_________________________________________________。
(5)在1 183 K以下,元素⑨形成如图甲所示基本结构单元的晶体;1 183 K以上,转变为图乙所示基本结构单元的晶体。

在1 183 K以下的晶体中,与元素⑨的原子等距离且最近的原子数为___________;在1 183 K以上的晶体中,与元素⑨原子等距离且最近的原子数为___________。
(B)“实验化学”课程模块
已知亚甲基蓝其氧化型呈蓝色,还原型呈无色,其转化关系式为:

氧化型(蓝色)+ne-![]() 还原型(无色)。
还原型(无色)。
奇妙的“蓝瓶子”实验就是利用上述原理,其装置如图甲。
某校化学兴趣小组用图甲装置进行下述实验:
①在250 mL锥形瓶中,依次加入
②塞紧橡皮塞,关闭活塞a、b,静置,溶液变为无色;
③打开活塞、振荡,溶液又变为蓝色;
④关闭活塞、静置,溶液又变为无色;
⑤以上步骤③④可重复多次。
请回答下列问题:
(1)若塞紧图甲中锥形瓶塞,并打开导管活塞a、b,从___________(填“左”或“右”)导管口通入足量氦气后,再关闭活塞a、b并振荡,溶液__________(填“能”或“不能”)由无色变为蓝色。
(2)如图乙所示:某学生将起初配得的蓝色溶液分装在A、B两支试管中,A试管充满溶液,B中有少量溶液,塞上橡皮塞静置片刻,两溶液均显无色。若再同时振荡A、B试管,溶液显蓝色的是___________试管。
(3)上述转化过程中葡萄糖的作用是_______________,亚甲基蓝的作用是______________。
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为______________。
(5)该实验中③④操作___________(填“能”或“不能”)无限次重复进行,理由是____________。
查看习题详情和答案>>本题对应于“物质结构与性质”选修模块的内容。
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
|
Z |
|
|
|
|
|||||||||||||
|
|
|
M |
L |
Q |
R |
|
|
||||||||||
|
D |
A |
|
|
T |
X |
Y |
|
||||||||||
|
E |
|
|
|
|
|
|
|
|
J |
|
|
|
|
|
|
|
|
(1)Y分别与D、E形成的化合物中熔点较高是_________(用具体物质的化学式表示)。
(2)LX2分子的电子式是_________,MY3分子是_________(填“极性分子”或“非极性分子”)。
(3)由J、L、R三种元素形成的某种配位化合物,常温下该化合物具有挥发性,化学式为J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是__________________; J(LR)4固态时属于_________晶体(填晶体类型)
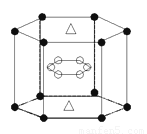
(4)A与M组成的一种化合物AM2,刷新了金属化合物超导温度的最
高记录。右图中所示的是该化合物的晶体结构单元。图中上,下
底面中心“Δ”处的原子是_______(填元素符号)。
查看习题详情和答案>>