摘要:27.A.B.C.D.E是中学常见单质.构成它们的元素的原子序数分别为a.b.c.d.e,且3 ,X.Y.Z.M.N.W.H.K是常见化合物.X是B和C的化合产物.它们之间有如下转化关系(图中反应物和产物中的H2O已略去): (1)X的电子式为 .构成D单质的元素在周期表中位于 周期 族. (2)反应③的离子方程式为 , E的氧化物与D在一定条件下反应的化学方程式为: . (3)固体K常温下即挥发.183℃升华.据此判断K为 型晶体. (4)K的水溶液和过量氨水反应的离子方程式为 . (5)25℃时.pH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为 .
网址:http://m.1010jiajiao.com/timu_id_1732822[举报]
A、B、C、D、E是中学常见的5种化合物,A、B是金属氧化物且A是红棕色固体,元素X、Y、Z是中学化学中常见的单质,相关物质间的关系如图所示.
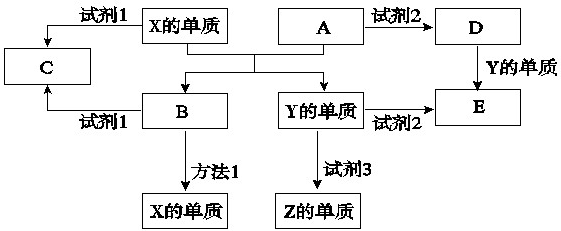
(1)工业上得到单质X的冶炼方法1是
(2)单质X与试剂1、单质Y与试剂2都能产生Z单质,试剂3是生活中常见的液体,请写出Y与试剂3反应的化学方程式是
(3)若试剂1是NaOH溶液,单质X与试剂1反应的离子方程式
(4)若试剂2是盐酸.
①如何检验D物质中的金属阳离子
②将D的饱和溶液滴加到沸水中得到有丁达尔效应的分散系,用离子方程式和平衡移动理论说明产生这种分散系的原因
查看习题详情和答案>>

(1)工业上得到单质X的冶炼方法1是
电解
电解
.(2)单质X与试剂1、单质Y与试剂2都能产生Z单质,试剂3是生活中常见的液体,请写出Y与试剂3反应的化学方程式是
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
.
| ||
(3)若试剂1是NaOH溶液,单质X与试剂1反应的离子方程式
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.(4)若试剂2是盐酸.
①如何检验D物质中的金属阳离子
取少量D溶液于试管中,再向试管中滴加少量的硫氰化钾溶液,若溶液显红色,则D物质中的金属阳离子是Fe3+
取少量D溶液于试管中,再向试管中滴加少量的硫氰化钾溶液,若溶液显红色,则D物质中的金属阳离子是Fe3+
.②将D的饱和溶液滴加到沸水中得到有丁达尔效应的分散系,用离子方程式和平衡移动理论说明产生这种分散系的原因
D溶液存在Fe3++3H2O?Fe(OH)3+3H+水解平衡,且正反应是吸热反应,当其滴加到沸水中时使平衡向正向移动,产生大量的Fe(OH)3凝结成胶体颗粒,而有丁达尔效应
D溶液存在Fe3++3H2O?Fe(OH)3+3H+水解平衡,且正反应是吸热反应,当其滴加到沸水中时使平衡向正向移动,产生大量的Fe(OH)3凝结成胶体颗粒,而有丁达尔效应
.A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,X、Y是生活中常见的金属单质,相关物质间的关系如下图所示.

请回答下列问题:
(1)写出X与A反应的化学方程式:
(2)若试剂1是NaOH溶液,写出X与试剂1反应的离子方程式
(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是
②将物质C溶于水,其溶液呈酸性,原因是
③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以D、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是
(4)若试剂1和试剂2均是稀盐酸,将C与D混合后,通入气体Z,再滴加氢氧化钠溶液调节溶液的pH,可水解聚合得到高效净水剂聚合氯化铝铁[AlFe(OH)nCl6-n]m.气体Z是
查看习题详情和答案>>

请回答下列问题:
(1)写出X与A反应的化学方程式:
3FeO+2Al
Al2O3+3Fe
| ||
3FeO+2Al
Al2O3+3Fe
.
| ||
(2)若试剂1是NaOH溶液,写出X与试剂1反应的离子方程式
2Al+2H2O+2OH-═2AlO2-+3H2↑
2Al+2H2O+2OH-═2AlO2-+3H2↑
.(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是
取少量溶液于试管中,滴加几滴KSCN溶液不变色,滴加氯水后溶液变红色,则证明原溶液中含有Fe2+
取少量溶液于试管中,滴加几滴KSCN溶液不变色,滴加氯水后溶液变红色,则证明原溶液中含有Fe2+
.②将物质C溶于水,其溶液呈酸性,原因是
Al3++3H2O  Al(OH)3+3H+
Al(OH)3+3H+
 Al(OH)3+3H+
Al(OH)3+3H+Al3++3H2O  Al(OH)3+3H+
Al(OH)3+3H+
(用离子方程式表示). Al(OH)3+3H+
Al(OH)3+3H+③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以D、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
.(4)若试剂1和试剂2均是稀盐酸,将C与D混合后,通入气体Z,再滴加氢氧化钠溶液调节溶液的pH,可水解聚合得到高效净水剂聚合氯化铝铁[AlFe(OH)nCl6-n]m.气体Z是
氯气
氯气
,其作用是亚铁离子氧化为铁离子
亚铁离子氧化为铁离子
.A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y、的单质是生活中常见的金属,相关物质间的关系如下图所示.

回答下列问题:
(1)X的单质与A反应的化学方程式是
(2)若C溶液显碱性,则试剂1是
(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是
②写出D-E反应的离子方程式
③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是(不必配平):
查看习题详情和答案>>

回答下列问题:
(1)X的单质与A反应的化学方程式是
Fe2O3+2Al
Al2O3+2Fe
| ||
Fe2O3+2Al
Al2O3+2Fe
.
| ||
(2)若C溶液显碱性,则试剂1是
NaOH(或KOH)
NaOH(或KOH)
溶液(写化学式);若C溶液显酸性,则显酸性的原因是(用离子方程式表示)Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是
取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+
取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+
;②写出D-E反应的离子方程式
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
;③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是(不必配平):
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
.
A、B、C、D、E是中学常见的五种物质,其转化关系如图所示;其中,反应Ⅰ在溶液中进行,其中某些生成物可能已略去。已知,A、E是短周期元素的单质,B、C、D是化合物,B是可溶性的一元强碱;A和D的水溶液具有漂白性。

(1)写出反应Ⅰ的离子方程式_____________________。
(2)在D的水溶液中,各离子的浓度由大到小的顺序是_____________。
(3)取2 mL 0.1 mol·L-1的AgNO3溶液,向其中滴加2 mL 0.1 mol·L-1的C溶液,现象是_____________;然后继续向其中滴加0.1 mol·L-1的KI溶液,能否观察到明显现象?(若有,请写出实验现象和反应的离子方程式;若没有,请简要说明原因。)
查看习题详情和答案>>(16分)A、B、C、D、E是中学常见的五种物质,其转化关系如下图示。反应I、II均在水溶液中进行,其中某些物质可能已略去。已知D是单质,C、E是化合物。
(1)若A是单质,其水溶液具有漂白性,D在常温下为固态,且A、D均可使湿润的淀粉碘化钾试纸变蓝。E是一种可溶性强碱,其焰色反应为黄色。
①E的电子式为 ;C固态时的晶体类型为 ;
②写出反应II的离子方程式 ;
③在E的环境中,A与B还可以发生另外一个反应,每1mol B完全反应转移6 mol电子,写出反应的化学方程式 。
(2)若B是单质,工业上用电解氧化物的方法获得B。B元素原子的电子层数等于其最外层电子数。D是无色无味的气体,E是B的最高价氧化物的水化物。
①若C溶液显酸性,其原因用离子方程式表示为 ;
②若C溶液显碱性,则反应II的离子方程式为 。
查看习题详情和答案>>