摘要:27.硫酸是基础化学工业的重要产品 (1)目前.我国采用“接触法 制硫酸.简单流程如图所示: ①B设备C中名称是 .图中b处导出气体的成分是 . ②设备C中用98.3%的H2SO4来吸收SO2的原因是 . ③燃烧It含硫质量分数为48%的黄铁矿石.在理论上能生产98%H2SO4 t. (2)工业上曾用煅烧绿矾(FeSO4·7H2O)的方法生产硫酸, 其中SO3与水蒸气同时冷凝便可得到硫酸.为了检验反应的部分产物进行如下实验: ①加热试管I中观察到的现象是 . ②若将试管II中的BaCl2溶液改为Ba(NO3)2溶液.能否确定有SO3生成.请简述理由: . 080601 ③I.II两试管口均塞有一团蘸有浓碱液的棉花.其目的是: .
网址:http://m.1010jiajiao.com/timu_id_1732786[举报]
有机物A是重要的化工原料.主要用于医药工业中,是合成药物的中间体,并可作为塑料、染料等产品的中间体.如图是合成有机物A的逆合成分析.

(1)经燃烧分析实验测定,有机物B中各元素的质量分数是碳52.2%,氢13.0%,氧34.8%.通过质谱法测定,B的相对分子质量为46.红外光谱表明B中有羟基O-H键,B的结构简式为
(2)合成有机物A的基础原料的结构简式为
(3)写出下列反应的化学方程式.
①
②
(4)有机合成后,必须测定其结构才能确定它是否就是目标产物.有机物A的核磁共振氢谱有
查看习题详情和答案>>

(1)经燃烧分析实验测定,有机物B中各元素的质量分数是碳52.2%,氢13.0%,氧34.8%.通过质谱法测定,B的相对分子质量为46.红外光谱表明B中有羟基O-H键,B的结构简式为
CH3CH2OH
CH3CH2OH
,(2)合成有机物A的基础原料的结构简式为
CH2=CH2
CH2=CH2
.(3)写出下列反应的化学方程式.
①

CH2ClCH2Cl+2NaOH
CH2OHCH2OH+2NaCl
| H2O |
CH2ClCH2Cl+2NaOH
CH2OHCH2OH+2NaCl
| H2O |
②

HOOCCOOH+2CH3CH2OH
CH3CH2OOC-COOCH2CH3+2H2O
| 浓硫酸 |
| △ |
HOOCCOOH+2CH3CH2OH
CH3CH2OOC-COOCH2CH3+2H2O
| 浓硫酸 |
| △ |
(4)有机合成后,必须测定其结构才能确定它是否就是目标产物.有机物A的核磁共振氢谱有
2
2
(填数字)种类型氢原子的吸收峰.(1)ag铁粉放入含bmolHNO3的浓硝酸中,加热充分反应后,再加入稀硫酸,铁粉恰好完全溶解,经测定溶液中只含Fe3+(一种金属离子)和SO42-(一种酸根离子).
①写出反应开始时溶液中发生反应的化学方程式______.
②写出加入硫酸后,所发生反应的离子方程式______.
(2)硫酸是基础化学工业的重要产品目前,我国采用“接触法”制硫酸,简单流程如图所示:
①设备B中名称是______,图中b处导出气体的成分是(写化学式)______.
②设备C中用98.3%的H2SO4来吸收SO2的原因是______.
③燃烧1t含硫质量分数为48%的黄铁矿石,在理论上能生产98%H2SO4______t.
查看习题详情和答案>>
(1)ag铁粉放入含bmolHNO3的浓硝酸中,加热充分反应后,再加入稀硫酸,铁粉恰好完全溶解,经测定溶液中只含Fe3+(一种金属离子)和SO42-(一种酸根离子).
①写出反应开始时溶液中发生反应的化学方程式______.
②写出加入硫酸后,所发生反应的离子方程式______.
(2)硫酸是基础化学工业的重要产品目前,我国采用“接触法”制硫酸,简单流程如图所示:

①设备B中名称是______,图中b处导出气体的成分是(写化学式)______.
②设备C中用98.3%的H2SO4来吸收SO2的原因是______.
③燃烧1t含硫质量分数为48%的黄铁矿石,在理论上能生产98%H2SO4______t.
查看习题详情和答案>>
①写出反应开始时溶液中发生反应的化学方程式______.
②写出加入硫酸后,所发生反应的离子方程式______.
(2)硫酸是基础化学工业的重要产品目前,我国采用“接触法”制硫酸,简单流程如图所示:

①设备B中名称是______,图中b处导出气体的成分是(写化学式)______.
②设备C中用98.3%的H2SO4来吸收SO2的原因是______.
③燃烧1t含硫质量分数为48%的黄铁矿石,在理论上能生产98%H2SO4______t.
(1)ag铁粉放入含bmolHNO3的浓硝酸中,加热充分反应后,再加入稀硫酸,铁粉恰好完全溶解,经测定溶液中只含Fe3+(一种金属离子)和SO42-(一种酸根离子).
①写出反应开始时溶液中发生反应的化学方程式
②写出加入硫酸后,所发生反应的离子方程式
(2)硫酸是基础化学工业的重要产品目前,我国采用“接触法”制硫酸,简单流程如图所示: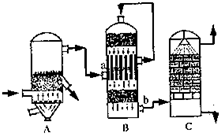
①设备B中名称是
②设备C中用98.3%的H2SO4来吸收SO2的原因是
③燃烧1t含硫质量分数为48%的黄铁矿石,在理论上能生产98%H2SO4
查看习题详情和答案>>
①写出反应开始时溶液中发生反应的化学方程式
Fe+4HNO3(浓)
Fe(NO3)2+2NO2↑+2H2O
| ||
Fe+4HNO3(浓)
Fe(NO3)2+2NO2↑+2H2O
.
| ||
②写出加入硫酸后,所发生反应的离子方程式
Fe+4H++NO3-═Fe3++NO↑+2 H2O; 3Fe2++4H++NO3-═3Fe3++NO↑+2 H2O
Fe+4H++NO3-═Fe3++NO↑+2 H2O; 3Fe2++4H++NO3-═3Fe3++NO↑+2 H2O
.(2)硫酸是基础化学工业的重要产品目前,我国采用“接触法”制硫酸,简单流程如图所示:

①设备B中名称是
接触室
接触室
,图中b处导出气体的成分是(写化学式)SO3、SO2、O2、N2
SO3、SO2、O2、N2
.②设备C中用98.3%的H2SO4来吸收SO2的原因是
为了提高SO3的吸收效率,防止形成酸雾
为了提高SO3的吸收效率,防止形成酸雾
.③燃烧1t含硫质量分数为48%的黄铁矿石,在理论上能生产98%H2SO4
1.5
1.5
t.[有机化学基础]2006年5月14日某新闻媒体报道齐齐哈尔第二制药有限公司生产的假药事件,“齐二药”违反规定,购入工业用“二甘醇”代替医用丙二醇(C3H8O2)作辅料,用于“亮菌甲素注射液”的生产,导致多名患者肾功能衰歇,造成多名患者死亡.二甘醇又称乙二醇醚,分子式为C4H10O3(HO-CH2-CH2-O-CH2-CH2-OH),二甘醇是一种重要的化工原料,可以制取酸、酯、胺等,其主要产品有吗啉及其衍生物1,4-二恶烷

请回答下列问题:
(1)下列关于“丙二醇”和“二甘醇”及“乙二醇”的有关说法正确的是
A.丙二醇是乙二醇的同系物
B.它们具有相同种类和数目的官能团,性质上完全相同
C.“丙二醇”和“二甘醇”在病人体内都能被氧化为草酸
D.分离“丙二醇”和“二甘醇”可采用分液的方法
(2)过程Ⅰ是石油加工中常用步骤,其名称为
(3)从物质B到物质C的过程如果条件控制不好会生成物质E,E可用于金属的切割,则为了能得到二甘醇D,物质B到物质C的反应条件是
(4)物质D是二甘醇,则合成路线中的物质A、B、C的结构简式分别是:
A:
(5)反应Ⅲ的化学方程式为:
(6)写出二甘醇制备1,4-二恶烷的化学方程式:
查看习题详情和答案>>
删除此空
删除此空
等被广泛应用于石油化工、橡胶、塑料、制药等行业,用途十分广泛.二甘醇一般的合成路线为:
请回答下列问题:
(1)下列关于“丙二醇”和“二甘醇”及“乙二醇”的有关说法正确的是
A.丙二醇是乙二醇的同系物
B.它们具有相同种类和数目的官能团,性质上完全相同
C.“丙二醇”和“二甘醇”在病人体内都能被氧化为草酸
D.分离“丙二醇”和“二甘醇”可采用分液的方法
(2)过程Ⅰ是石油加工中常用步骤,其名称为
裂解
裂解
.(3)从物质B到物质C的过程如果条件控制不好会生成物质E,E可用于金属的切割,则为了能得到二甘醇D,物质B到物质C的反应条件是
氢氧化钠水溶液、加热
氢氧化钠水溶液、加热
,该反应属于取代反应
取代反应
(添反应类型).写出B可能生成E的化学方程式:CH2BrCH2Br+2NaOH
HC≡CH↑+2NaBr
| 醇 |
| △ |
CH2BrCH2Br+2NaOH
HC≡CH↑+2NaBr
.| 醇 |
| △ |
(4)物质D是二甘醇,则合成路线中的物质A、B、C的结构简式分别是:
A:
C2H2
C2H2
B:BrCH2CH2Br
BrCH2CH2Br
C:HOCH2CH2OH
HOCH2CH2OH
(5)反应Ⅲ的化学方程式为:
2HO-CH2-CH2-OH
2HO-CH2-CH2-O-CH2-CH2-OH+H2O
| 浓硫酸 |
| △ |
2HO-CH2-CH2-OH
2HO-CH2-CH2-O-CH2-CH2-OH+H2O
.| 浓硫酸 |
| △ |
(6)写出二甘醇制备1,4-二恶烷的化学方程式:
HO-CH2-CH2-O-CH2-CH2-OH
 +H2O
+H2O
| 浓硫酸 |
| △ |
 +H2O
+H2OHO-CH2-CH2-O-CH2-CH2-OH
 +H2O
+H2O
.| 浓硫酸 |
| △ |
 +H2O
+H2O