摘要:13.如下图所示的两个实验装置中.溶液的体积均为200mL.开始时电解质溶液的浓度均为0.1mol/L.工作一段时间后.测得两个装置中均通过0.02mol电子时(不考虑盐的水解和溶液体积的变化)则下列叙述中正确的是 A.电极上析出物质的质量:①=② B.溶液的pH变化:①增大.②不变 C.电极反应式:①中阳极 2Cl--2e- Cl2 ↑ ②中负极 2H++2e- H2↑ D.产生气体的体积:①=② 第Ⅱ卷 非选择题 ,3,5 26.下表是短周期中部分元素的原子半径及主要化合价. 元素代号 U V W X Y Z 原子半径/nm 0.037 0.157 0.066 0.070 0.077 0.143 主要化合价 +1 +1 -2 -3,+5 +2,+4 +3 请回答: (1)Y在元素周期表中的位置是 .镁条在盛有YW2气体的集气瓶中燃烧的现象为 . (2)V.W.Z三种元素的离子具有相同的电子层结构.三者的离子半径由大到小顺序是 . 并用离子方程式表示出Z离子可作净水剂的原因 (3)W.X.Y分别与U可形成10电子共价化合物.三者均可形成 晶体.其中沸点最高的是 ,1g YU4气体完全燃烧生成液态水时.放出a kJ的热量,则该反应的热化学方程式为 . (4)现有Z与V2W2的固体混合物样品.加入稀盐酸至混合物完全溶解.所得的混合液中c(Z3+)︰c(H+)︰c(Cl-)=1︰2︰8.则原固体混合物中.Z元素与W元素的质量比为 .
网址:http://m.1010jiajiao.com/timu_id_1732700[举报]
如下图所示的两个实验装置中,溶液的体积均为200 mL,开始时电解质溶液的浓度均为0.1 mol·L-1,工作一段时间后,测得导线中均通过0.02 mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
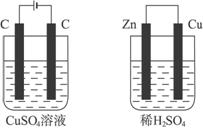
① ②
A.产生气体的体积:①>②
B.电极上析出物质的质量:①>②
C.溶液的pH变化:①增大,②减小
D.电极反应式①中阳极:4OH--4e![]() 2H2O+O2↑ ②中负极:2H++2e-
2H2O+O2↑ ②中负极:2H++2e-![]() H2↑
H2↑
如下图所示的两个实验装置中,溶液的体积均为200 mL,开始时电解质溶液的浓度均为0.1 mol·L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )

A.产生气体的体积:①>②
B.电极上析出物质的质量:①>②
C.溶液的pH变化:①增大,②减小
D.电极反应式:①中阳极:4OH--4e-====2H2O+O2↑;②中负极:2H++2e-====H2↑
查看习题详情和答案>>如下图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,则下列叙述中正确的是( )
A.产生气体的体积:①>②
B.溶液的pH变化:①不变 ②增大
C.①和②中铜电极均失电子
D.电极反应式:①中阳极 ![]() ②中负极
②中负极 ![]()
查看习题详情和答案>>

 ②中负极
②中负极 
