网址:http://m.1010jiajiao.com/timu_id_1732472[举报]
已知a、b、I、K四种粒子都有10个电子,其结构特征如下:

A可作为工业上生产酸J的原料,B、C为非金属单质,E为红棕色固体,物质D由a、b构成,G是一种消毒剂的主要成分.各物质之间的转化关系如下图所示(个别产物略去).
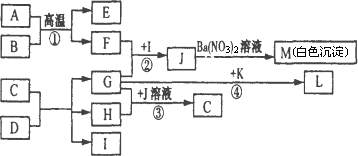
请回答下列问题:
(l)考虑到综合经济效益,工业生产K时,可采取的措施有________(填序号).a.使用催化剂 b.适当降低温度 c.适当增大压强 d.及时分离出产物 e.对原料进行循环利用 f.充分利用反应本身放出的热量 g.工厂地址选择在交通发达的大城市
(2)写出反应②的离子方程式:________________.
(3)反应④中,G(溶液)与K能以物质的量之比为1∶2反应生成L、H、I.L是一种火箭燃料,其分子中各原子均已达稳定结构.则L的电子式为________,该反应的化学方程式为________________.
(4)将F通入含等物质的量的D的溶液中,反应后的溶液能使甲基橙显红色,则此溶液中各微粒浓度的守恒关系是________________(只写一种).
(5)工业上反应①应在________(填设备名称)中进行.现有1 mol A参加反应,假设各步均反应完全,生成M的质量为1165 g,生成E的质量为320 g,则反应①的化学反应方程式为________________.
已知a、e、I为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
|
粒子代码 |
a |
e |
I |
|
原子核数 |
单核 |
两核 |
四核 |
|
粒子的电荷数[来源:学,科,网Z,X,X,K] |
一个单位正电荷 |
一个单位负电荷 |
0 |
物质A由a、e 构成, B、C、D、K都是单质,各有关物质之间的相互反应转化关系如下图所示,反应①—⑤ 都是用于工业生产的反应,⑥、⑦反应中个别产物在图中略去。
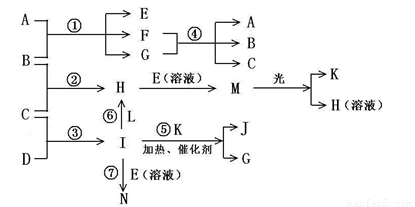
请填写下列空白:
(1)写出下列物质的化学式:B__________,J__________。
(2)写出下列反应的离子反应方程式:
H + E(溶液)→M____________________________________________________,
F + G →A + B + C________________________________________;
(3)E(溶液)能与I以1∶2的物质的量之比反应生成N、F和G,N中各原子均已达到惰性气体的稳定结构,写出N的结构式__________;
(4)L是由3种元素构成的分子,能与I以1∶2的物质的量之比反应生成尿素CO(NH2) 2 和物质H,写出L的电子式__________;
(5)反应③用于工业生产它应在_______________进行(填设备名称);反应④用于工业生产时为了防止B和C混合反应产生危险,所使用的一种特殊材料的名称为__________,在该工业生产中它具有的特殊的性质是________________________。
(6)常温下,实验室模拟工业反应④的过程如下图所示,标况下,当电极上产生112mL(已折算为标准状况下的体积)B气体时,烧杯中溶液的pH=__________。(假设气体完全逸出,溶液体积不变)
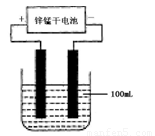
查看习题详情和答案>>
| 粒子代码 | a | e | I |
| 原子核数 | 单核 | 两核 | 四核 |
| 粒子的电荷数 | 一个单位正电荷 | 一个单位负电荷 |
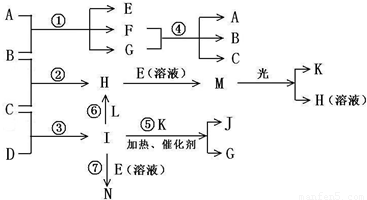
(1)写出下列物质的化学式:B______,J______.
(2)写出下列反应的离子反应方程式:H+E(溶液)→M______,F+G→A+B+C______ Cl2+H2+2OH- 查看习题详情和答案>>
已知a、I、e为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
| 粒子代码 | a | I | e |
| 原子核数 | 单核 | 四核 | 双核 |
| 粒子的电荷数 | 一个单位正电荷 | 0 | 一个单位负电荷 |

请填写下列空白:?
(1)写出下列物质的化学式:B J 。
(2)写出下列反应的离子方程式:
①H+E(溶液)→M 。?②I溶于G 。
(3)在通常状况下,若1 g C气体在B气体中燃烧生成H气体时放出92.3 kJ热量,则2 mol H气体完全分解生成C气体和B气体的热化学方程式为 。 查看习题详情和答案>>
已知a、I、e为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
|
粒子代码 |
a |
I |
e |
|
原子核数 |
单核 |
四核 |
双核 |
|
粒子的电荷数 |
一个单位正电荷 |
0 |
一个单位负电荷 |
物质A由a、e构成,B、C、D、K都是单质,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:

请填写下列空白:?
(1)写出下列物质的化学式:B J 。
(2)写出下列反应的离子方程式:
①H+E(溶液)→M 。?②I溶于G 。
(3)在通常状况下,若1 g C气体在B气体中燃烧生成H气体时放出92.3 kJ热量,则2 mol H气体完全分解生成C气体和B气体的热化学方程式为 。
查看习题详情和答案>>