摘要:29.下图每一方框中的字母代表一种反应物或生成物. (1)若X由M.N两种短周期且同周期元素形成 .M原子的最外层电子数是最内层电子数的N元素最高正价与它的负价代数和为6. ①写出反应Ⅱ的离子方程式 . ②右图为IV达到平衡后改变反应条件.反应速率随时间变化的情况.已知t2-t3阶段为便用催化剂,t3-t4阶段为减小体系的压强.写出符合上述条件的化学方程式 (写一个即可.用具体物质表示),若t4-t5阶段为升高体系的温度.则该反应为 ③某温度下.四个容器中均进行着上述反应.各物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中相应的空格. 容器编号 C(C)/mol·L-1 C(D)/mol·L-1 C(G)/mol·L-1 V正.V逆比较 甲 0.06 0.60 0.60 V正=V逆 乙 0.6 0.50 0.40 丙 0.12 0.40 0.80 V正<V逆 丁 0.12 0.30 V正=V逆 (2)若X是一种含氧酸盐.B是金属单质.C.D是非金属单质.反应Ⅱ需要B与A的浓溶液共热才能进行.且生成的E与G是同一种物质.写出反应Ⅰ的化学方程式 ,4g固态D在C中完全反应放出37.2kJ的热量.写出该反应的热化学方程式 .
网址:http://m.1010jiajiao.com/timu_id_1732274[举报]
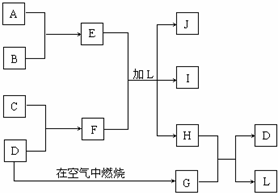 下图每一方框中的字母代表一种反应物或生成物:
下图每一方框中的字母代表一种反应物或生成物:产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质.试填写下列空白:
(1)L的化学式为:
H2O
H2O
.(2)F的化学式为:
Na2S
Na2S
.(3)写出J受热分解反应的化学方程式:
2Al(OH)3
Al2O3+3H2O
| ||
2Al(OH)3
Al2O3+3H2O
.
| ||
(4)H和G之间反应的化学方程式为:
2H2S+SO2═3S+2H2O
2H2S+SO2═3S+2H2O
.下图每一方框中的字母代表一种反应物或生成物:
物质A跟B反应生成物质E、F和G;物质C跟D反应生成物质I,某温度下该反应起始和某时刻的反应混合物组成如右上表格所示.请填写下列空白:
(1)物质H的分子式是
(2)反应①的化学方程式是
(3)反应②的化学方程式(须注明反应条件)是
查看习题详情和答案>>

物质A跟B反应生成物质E、F和G;物质C跟D反应生成物质I,某温度下该反应起始和某时刻的反应混合物组成如右上表格所示.请填写下列空白:
(1)物质H的分子式是
HCl
HCl
.(2)反应①的化学方程式是
Cl2+2NaOH=NaClO+NaCl+H2O
Cl2+2NaOH=NaClO+NaCl+H2O
.(3)反应②的化学方程式(须注明反应条件)是
N2+3H2
2NH3
| ||
| 高温高压 |
N2+3H2
2NH3
.
| ||
| 高温高压 |
下图每一方框中的字母代表一种反应物或生成物,它们都是中学化学中常见的物质.产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,L是水,D是淡黄色固体,E为单质.试填写下列空白:
(1)写出F的化学式:
(2)写出M发生水解的化学反应方程式

查看习题详情和答案>>
(1)写出F的化学式:
CO2
CO2
.(2)写出M发生水解的化学反应方程式
CO32-+H2O═HCO3-+OH-
CO32-+H2O═HCO3-+OH-
. (3)反应C+G→D的化学方程式是2Na+O2
Na2O2
| ||
2Na+O2
Na2O2
. (4)写出H、K加L生成J、I、F反应的离子方程式
| ||
Al3++3HCO3-═Al(OH)3↓+3CO2↑
Al3++3HCO3-═Al(OH)3↓+3CO2↑
.
下图每一方框中的字母代表一种反应物或生成物(图中部分反应物或生成物没有列出)。其中,化合物石灰氮是由钙、碳等三种元素组成的盐,它以前是一种常用的肥料,其含钙、碳的质量分数分别为50%、15%。反应①是石灰氮的完全水解,其产物之一可方便地制成一种氮肥。通常状况下,C为气体。

请按要求回答:
(1)写出石灰氮的化学式_____________。
(2)写出反应①的化学方程式_____________________________________________。
(3)除反应②③④⑤是应用于工业生产外,还有两个是应用于工业生产的反应,是_________和___________(填代号),它们反应的化学方程式分别是______________________________和_____________________________________________。
查看习题详情和答案>>