网址:http://m.1010jiajiao.com/timu_id_1732264[举报]
| (1) 草酸晶体 | 分子式 | H2C2O4·2H2O | 颜色 | 无色晶体 |
| 熔点 | 100.1℃ | 受热至100.1℃时失去结晶水,成为无水草酸。 | ||
| (2) 无水草酸 | 结构简式 | HOOC—COOH | 溶解性 | 能溶于水或乙醇 |
| 特性 | 大约在157℃升华(175℃以上发生分解)。 | |||
| 化学性质 | H2C2O4 + Ba(OH)2 =BaC2O4↓+ 2H2O | |||
| HOOC—COOH >175℃ CO2↑+CO↑+H2O↑ | ||||
该组同学依据上表设计了一套如下图所示的实验装置,欲通过实验验证无水草酸受热分解的产物,并利用反应产生的CO气体来还原铁的某种氧化物(FexOy),以确定FexOy的组成。

请回答下列问题:
(1)实验所需的仪器装置如上图所示,各装置的连接顺序为:
e接 、 接 、 接 、 接 h 。
(2)该组同学进行了下列实验操作:
①点燃B处的酒精灯;
②检查实验装置的气密性并装入药品;
③反应结束后,先熄灭B处的酒精灯,继续通入气体直到B中固体全部冷却后,再熄灭c处的酒精灯;
④点燃c处的酒精灯,开始反应,在装置E的i口处收集一试管气体,验纯;
⑤点燃尖嘴i处的酒精灯。
正确的实验操作顺序是: 。
(3)收集气体验纯的目的是 。
D装置中澄清石灰水的作用是 。
E装置中澄清石灰水的作用是 。
(4)反应完全后,该组同学进行数据处理。反应前,称得硬质玻璃管的质量为54.00 g,样品FexOy的质量为7.84 g;反应后,称得硬质玻璃管与剩余固体的总质量为59.60g(其质量经同样操作后也不再发生变化),则样品FexOy中,x:y= 。
(5)本实验有没有不妥之处?如果有,请答出改进的方案;若无,此问可不必答。
。
请完成下列各题:
(1)前4周期中,基态原子中未成对电子数为4的元素原子的电子排布式为________________。
(2)NaCl晶体中,与Na+等距离且最近的Na+有________________个。
(3)N 原子的第一电离能___________(填 “>”“<” 或“=”)O原子的第一电离能,N2分子中存在_______个σ键和_______个π键,NH3的沸点比PH3_________(填“高”或“低”),![]() 中N原子的杂化方式为________________,
中N原子的杂化方式为________________,![]() 的空间构型为________________。
的空间构型为________________。
1.已知次溴酸(HBrO)的结构简式为HO—Br,如图乙烯跟溴水中各成分反应既可生成A,同时又可生成B和C2H5Br。

回答下列问题:
(1)环氧乙烷![]() 的结构可简写为
的结构可简写为![]() ,则E的化学式是__________。
,则E的化学式是__________。
(2)A的结构简式是__________;I的结构简式是__________。
(3)写出G转化为H的化学方程式________________________。其反应类型为__________反应。
(4)化合物A—I中,易发生加成反应的物质是__________(填字母)。
2.(一)(1)科技日报
A.Al2H6中H为+1价,Al为-3价
B.Al2H6在空气中完全燃烧,产物为氧化铝和水
C.氢铝化合物Al2H6的晶体为分子晶体
D.氢铝化合物可能成为未来的储氢材料和火箭燃料
(二)A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A、B两元素的核电荷数之差等于它们的原子最外层电子数之和;F元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E、F形成的化合物甲、乙、丙、丁、戊、己的组成如下表所示。
化合物 | 甲 | 乙 | 丙 | 丁 | 戊 | 己 |
化学式 | A | A | B | D | A2E | DF |
回答下列问题:
(2)化合物丁的电子式为__________。F原子的最外层电子排布式为__________。
(3)化合物戊的沸点比甲__________(填“高”或“低”),写出甲与丁反应的化学方程式:____________________。
(4)
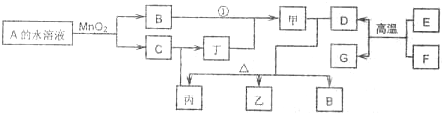
(1)A的结构式为
(2)若反应①除生成甲外,还生成丙,写出过量D与甲的稀溶液反应时的离子方程式:
(3)以D、F为电极.NaOH溶液为电解质溶液可以组成原电池.该原电池负极的电极反应式为
(4)若A与丙可以化合生成甲;甲的稀溶液和浓溶液分别与D在一定条件下反应可以生成组成组成元素完全不同的两种气体和其他物质.请写出A与丙化合生成甲的化学反应方程式:
A 、B 、C 、D 、E 、F、G为原子序数依次增大的元素,其中前六种属于短周期元素。已知B 、C 、F 三种原子的最外层共有11 个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应并且生成盐和水。请完成下列问题:
(1)只根据以上条件一定能判断出的元素的及符合条件的离子的符号填写在下表空格处
| 编号 | A | B | C | D | E | F | G | 半径最小的离子 |
| 符号 |
 (2)写出B、C 的最高价氧化物对应的水化物间反
(2)写出B、C 的最高价氧化物对应的水化物间反
应的离子方程式____________
(3)己知D的单质在F单质中燃烧可生成X、Y两
种化合物并产生白色烟雾,写出X、Y中各原子
最外层均满足8 电子结构的分子的电子式___。
D、F的单质反应过程和能量关系如图所示(图
中的△H表示生成1mol产物的数据),写出指定
条件下两种单质作用生成Y时的热化学方程式
_______________________。
(4) G的单质是目前用途最广泛的一种金属材料,但在使用中受环境影响易被腐蚀,试写出发生腐蚀时的电极反应式_________________________________________。
(5)A与E能形成两种常见的化合物,这两种化合物中属于非极性分子的物质化学式_______
查看习题详情和答案>>