网址:http://m.1010jiajiao.com/timu_id_1731739[举报]
铜有Cu2O(红色)和CuO(黑色)两种常见的氧化物。某高中化学兴趣小组的同学对初中课本实验的结论“H2与CuO反应生成红色物质Cu”提出质疑,认为生成的红色物质不一定就是铜。为了确定该红色物质的成分,该兴趣小组开展了以下研究。
(一)提出猜想:红色物质可能是铜、氧化亚铜或两者的混合物。
(二)查阅资料:①Cu2+在酸性条件下能发生自身氧化还原反应(Cu2O+2H+ =Cu2++Cu+H2O);②在空气中灼烧Cu2O能生成CuO。
(三)制备红色物质:方法同初中课本
(四)红色物质成分的探究:
甲同学设计了以下三种探究方案:
方案I:取该红色物质溶于足量稀硝酸中,观察溶液颜色的变化。
方案II:取该红色物质溶于足量稀硫酸中,观察现象。
方案III:称得干燥的坩埚的质量为m1g,取红色物质置于坩埚中再称得质量为m2g。
然后将红色物质在空气中充分灼烧至完全变黑,并在干燥器中冷却,再称量,反复多次直到质量不变,称得最后质量为m3g,比较m1、m2、m3。
回答下列问题:
(1)方案I是否合理 (填“合理”或“不合理”)。如果你认为该方案合理,请简述其工作原理;如果你认为该方案不合理,请简述原因。 。
(2)方案II中,若观察不到明显现象,则可知红色物质为 ;若观察到溶液变为蓝色,则可知红色物质为 。
(3)方案III中,如果m1、m2、m3的关系符合m3= ,可确认红色物质为Cu2O。
(4)乙同学利用下列装置设计了第四种探究方案:

各装置接口的正确连接顺序是( )接( )( )接( )( )接( );试剂X可选用 ;要测定红色物质的成分,最少需要测定的物理量是 (填序号)。
①通入氢气的体积 ②反应前,红色物质+反应管的总质量
③实验前干燥管的质量 ④完全反应后,红色物质+反应管的总质量
⑤反应管的质量 ⑥实验后干燥管的质量
查看习题详情和答案>>①提出假设:
假设Ⅰ:若过氧化钠氧化二氧化氮(反应只生成一种盐),则发生反应:
假设Ⅱ:若二氧化氮氧化过氧化钠(反应生成一种盐和一种气体单质),则发生反应:
②查阅资料:a.亚硝酸钠在酸性条件下能发生自身氧化还原反应:2NaNO2+2HCl═2NaCl+H2O+NO2↑+NO↑;
b.检验NO
- 3 |
- 3 |
| ||
③设计实验:
a.在一瓶集气瓶里充满红棕色的二氧化氮,用药匙放进一勺淡黄色的过氧化钠粉末,盖上毛玻璃片用力振荡,用手摸瓶壁感觉发烫,红棕色迅速消失了;
b.反应完后,用带火星的木条伸入瓶内,木条不复燃;
c.向反应后的残余物中加入盐酸,无明显现象;
d.将瓶内固体充分溶解,浓缩,再加入浓硫酸和铜粉共热,可产生红棕色有刺激性气味的气体,且溶液呈蓝色.
④实验结论:假设
B、已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验.
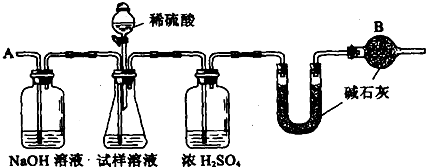
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到b g
④从分液漏斗滴入6mol?L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到c g
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为d g
请填空和回答问题:
(1)装置中干燥管B的作用是
(2)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果
(3)步骤⑤的目的是
(4)步骤⑦的目的是
(5)该试样中纯碱的质量分数的计算式为
| 106(d-b) |
| 44a |
| 106(d-b) |
| 44a |