网址:http://m.1010jiajiao.com/timu_id_1731267[举报]
(1)工业上用NaCl还原NaClO3生产ClO2的工艺流程如下图所示:

①反应器中发生反应的化学方程式为:
2NaClO3+2NaCl+2H2SO4![]() 2ClO2↑+Cl2↑+2Na2SO4+2H2O
2ClO2↑+Cl2↑+2Na2SO4+2H2O
生产中将NaClO3和NaCl按物质的量之比1∶1.05的混合水溶液加入反应器,NaCl稍过量的目的是___________________________________________________________________。
②反应器中生成的ClO2和Cl2由通入空气驱出进入ClO2吸收塔,产生的混合液进入汽提塔,汽提塔排出的废液成分主要是______________(填化学式,下同)。
③以上生产流程中循环②循环利用的物质是______________。
④为提高ClO2的产量,可用亚氯酸钠(NaClO2)与反应器中的Cl2反应生成ClO2,该反应的化学方程式为________________________________________________。尾气中的Cl2可用SO2水溶液吸收,该反应的化学方程式为_____________________________________________。
(2)用阳离子交换膜分隔的电解池电解
A.电解时电子流向为:电源负极→导线→阴极,阳极→导线→电源正极
B.在电解过程中,Na+向阳极移动,![]() 向阴极移动
向阴极移动
C.在电解过程中阳极周围的pH基本不变
D.电解的离子方程式可表示为:2![]() +2H2O
+2H2O![]() 2ClO2↑+H2↑+2OH-
2ClO2↑+H2↑+2OH-
二氧化氯(ClO2)被称作第四代杀菌消毒剂。工业上用NaCl 还原NaClO3生产ClO2的工艺流程如图所示:

(2)生产中将NaClO3和NaCl按物质的量之比1:1.05的混 合水溶液加入反应器。NaCl稍过量的目的是____________。
(3)制取ClO2可用阳离子交换膜分隔的电解池电解NaClO2溶液,在阳极室加入的物质是___________,在阴极室产生的物质是________,电解的离子方程式可表示为______。
二氧化氯(ClO2)被称作第四代杀菌消毒剂。
(1)工业上用NaCl还原NaClO3生产ClO2的工艺流程如下图所示:
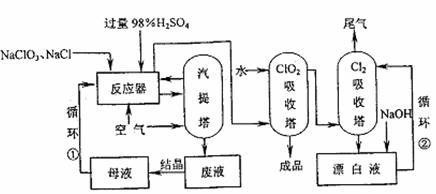
①反应器中发生反应的化学方程式为:
2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O
生产中将NaClO3和NaCl按物质的量之比1:1.05的混合水溶液加入反应器,NaCl稍过量的目的是 。
②反应器中生成的ClO2和Cl2由通入空气驱出进入ClO2吸收塔,产生的混合液进入汽提塔,汽提塔排出的废液成分主要是 (填化学式,下同)。
③以上生产流程中循环②循环利用的物质是 。
④为提高ClO2的产量,可用亚氯酸钠(NaClO2)与反应器中Cl2反应生成ClO2,该反应的化学方程式为 。尾气中的Cl2可用SO2水溶液吸收,该反应的化学方程式为 。
(2)用阳离子交换膜分隔的电解池电解450g/L NaClO2溶液,可在阳极室产生ClO2,在阴极室产生H2和NaOH。下列有关说法正确的是 (填字母符号)。
A.电解时电子流向为:电源负极→导线→阴极,阳极→导线→电源正极
B.在电解过程中,Na+向阳极移动,ClO2― 向阴极移动
C.在电解过程中阳极周围的pH基本不变
D.电解的离子方程式可表示为:2ClO2―+2H2O ![]() 2ClO2↑+H2↑+2OH―
2ClO2↑+H2↑+2OH―
漂白粉、漂白液、二氧化氯等含氯消毒剂是使用得最多的一类消毒剂。二氧化氯(ClO2)被称作第四代杀菌消毒剂,某化学工业公司用NaCl还原NaClO3生产ClO2的工艺流程如下图所示:

(1)反应器中发生反应的化学方程式为:
2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O
生产中将NaClO3和NaCl按物质的量之比1∶1.05的混合水溶液加入反应器,NaCl稍过量的目的是 。
(2)以上生产流程中循环②循环利用的物质是 。
(3)为提高ClO2的产量,可用亚氯酸钠(NaClO2)与反应器中的Cl2反应生成ClO2,另一产物是一常见化合物,完成该反应的化学方程式 。
查看习题详情和答案>>