网址:http://m.1010jiajiao.com/timu_id_1730641[举报]
 Ⅰ.X、Y、Z是短周期元素的三种常见氧化物.X跟水反应可生成一种具有还原性的不稳定的二元酸,该酸的化学式是______;Y和X组成元素相同,Y与水反应生成M,足量M的浓溶液与3.2g Cu在加热条件下充分反应,其中被还原的M的物质的量为______.固态Z可应用于人工降雨,0.5mol?L-1Z与NaOH反应所得的正盐水溶液中,离子浓度从大到小的顺序为______.
Ⅰ.X、Y、Z是短周期元素的三种常见氧化物.X跟水反应可生成一种具有还原性的不稳定的二元酸,该酸的化学式是______;Y和X组成元素相同,Y与水反应生成M,足量M的浓溶液与3.2g Cu在加热条件下充分反应,其中被还原的M的物质的量为______.固态Z可应用于人工降雨,0.5mol?L-1Z与NaOH反应所得的正盐水溶液中,离子浓度从大到小的顺序为______.
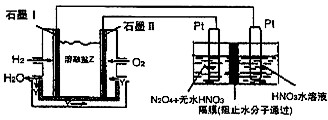
Ⅱ.N2O5是一种新型硝化剂,其性质和制备受到人们的关注.现以H2、O2、熔融盐Na2CO3组成的燃料电池,其中Y为CO2;采用电解法制备N2O5,总的反应方程式为:N2O4+2HNO3=2N2O5+H2,装置如图所示.
写出石墨I电极上发生反应的电极反应式______.
在电解池中生成N2O5的电极反应式为______.
Ⅲ.烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.
(1)烟气脱硫、脱硝对环境的意义______.
(2)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1.
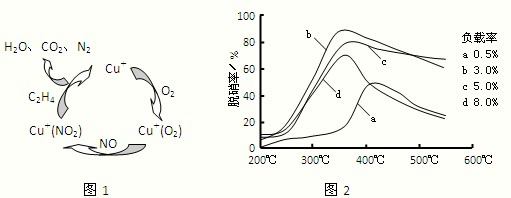
脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.
①写出该脱硝原理总反应的化学方程式:______.②为达到最佳脱硝效果,应采取的条件是______.
查看习题详情和答案>>
Ⅱ.N2O5是一种新型硝化剂,其性质和制备受到人们的关注.现以H2、O2、熔融盐Na2CO3组成的燃料电池,其中Y为CO2;采用电解法制备N2O5,总的反应方程式为:N2O4+2HNO3=2N2O5+H2,装置如图所示.
写出石墨I电极上发生反应的电极反应式______.
在电解池中生成N2O5的电极反应式为______.
Ⅲ.烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.
(1)烟气脱硫、脱硝对环境的意义______.
(2)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1.

脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.
①写出该脱硝原理总反应的化学方程式:______.②为达到最佳脱硝效果,应采取的条件是______.

Ⅱ.N2O5是一种新型硝化剂,其性质和制备受到人们的关注.现以H2、O2、熔融盐Na2CO3组成的燃料电池,其中Y为CO2;采用电解法制备N2O5,总的反应方程式为:N2O4+2HNO3=2N2O5+H2,装置如图所示.
写出石墨I电极上发生反应的电极反应式______.
在电解池中生成N2O5的电极反应式为______.
Ⅲ.烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.
(1)烟气脱硫、脱硝对环境的意义______.
(2)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1.

脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.
①写出该脱硝原理总反应的化学方程式:______ 3N2+4CO2+4H2O
 查看习题详情和答案>>
查看习题详情和答案>>
 Ⅰ.X、Y、Z是短周期元素的三种常见氧化物.X跟水反应可生成一种具有还原性的不稳定的二元酸,该酸的化学式是
Ⅰ.X、Y、Z是短周期元素的三种常见氧化物.X跟水反应可生成一种具有还原性的不稳定的二元酸,该酸的化学式是Ⅱ.N2O5是一种新型硝化剂,其性质和制备受到人们的关注.现以H2、O2、熔融盐Na2CO3组成的燃料电池,其中Y为CO2;采用电解法制备N2O5,总的反应方程式为:N2O4+2HNO3=2N2O5+H2,装置如图所示.
写出石墨I电极上发生反应的电极反应式
在电解池中生成N2O5的电极反应式为
Ⅲ.烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点.
(1)烟气脱硫、脱硝对环境的意义
(2)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1.

脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.
①写出该脱硝原理总反应的化学方程式:
| ||
| ||
M、R都是生活中常见的金属单质,其中R是用量最多的金属。甲、乙是化合物,其中甲是黑色晶体,可由R在x中燃烧得到。

(1)M与甲在高温下反应的化学方程式是
(2)电解法制R的低价氢氧化物的装置如图I。a是4 mol·L— NaCl、1mol·L—NaOH的混合溶液。
①配制a时需要除去蒸馏水中溶解的O2,常采用 的方法。
②石墨电极应与电源的 (填“正”或“负”)极相连接,通电后,R电极附近的现象是 ,
R极的电极反应式是 。
③停止实验一段时间后,在R极上部有红褐色物质产生,反应的化学方程式是 。
(3)把R的某氧化物粉末与M粉末混合后分成两等份。一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体质量比是a:b,则R的氧化物的化学式是 。
(4)如图是一个化学过程的示意图。
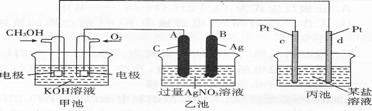
写出通入CH3OH的电极的电极反应式
(5)当乙池中B(Ag)极的质量增加5.40 g 时,甲池中理论上消耗O2 ml
(标准状况下);此时丙池某电极析出1.60 g某金属,则丙中的某盐溶液可能是 (填序号)。
A.MgSO4溶液 B.CuSO4溶液 C.NaCl溶液 D.AgN03溶液
查看习题详情和答案>>