摘要:12.某酸的酸式盐水溶液显碱性.下列有关叙述正确的是 ( ) A.的电离方程式为:H2Y 2H++Y2- B.在该盐的溶液里.离子浓度为: C.在该盐的溶液里.离子浓度为: D.水解的离子方程式为:HY-+H2O H2O++Y2-
网址:http://m.1010jiajiao.com/timu_id_1730588[举报]
下列有关叙述中不正确的是
![]() A.某酸式盐NaHY的水溶液显碱性,则
A.某酸式盐NaHY的水溶液显碱性,则![]() 的电离方程式为H2Y H++HY-
的电离方程式为H2Y H++HY-
B.Na2CO3溶液中存在:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
C.在由水电离出的c(H+)=lxl0-14m01·L-1的溶液中,可以大量存在Na+、K+、NO3-、HCO3-
D.在常温下,向10mLpH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20mL
查看习题详情和答案>>下列有关叙述中不正确的是


A.某酸式盐NaHY的水溶液显碱性,则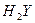 的电离方程式为H2Y H++HY- 的电离方程式为H2Y H++HY- |
| B.Na2CO3溶液中存在:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| C.在由水电离出的c(H+)=lxl0-14m01·L-1的溶液中,可以大量存在Na+、K+、NO3-、HCO3- |
| D.在常温下,向10mLpH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20mL |
某酸的酸式盐NaHY的水溶液显碱性,下列有关叙述正确的是( )
A.H2Y在电离时为:H2Y ![]() 2H++Y2-
2H++Y2-
B.在该盐的溶液里,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C.在该盐的溶液里,离子浓度为:c(Na+)>c(HY-) >c(H+) >c(Y2-)
D.HY水解的化学方程式为HY-+H2O![]() H3O++Y2-
H3O++Y2-
下列有关叙述中不正确的是
A.某酸式盐NaHY的水溶液显碱性,则 的电离方程式为H2Y H++HY- 的电离方程式为H2Y H++HY- |
| B.Na2CO3溶液中存在:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| C.在由水电离出的c(H+)=lxl0-14m01·L-1的溶液中,可以大量存在Na+、K+、NO3-、HCO3- |
| D.在常温下,向10mLpH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20mL |
现有下列10种物质
①NaHCO3;②NH4HCO3;③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食盐水;⑧CH3COOH; ⑨HCl;=10 ⑩NaOH.
(1)其中属于非电解质的是 (填序号,下同),既能跟盐酸反应又能跟NaOH溶液反应的是 .
(2)NaHCO3溶液显 性(填“酸”、“碱”或“中”),原因是(结合离子方程式表示)
.
(3)常温时有四种溶液:Ⅰ.pH=4的CH3COOH溶液;Ⅱ.pH=4的HCl溶液;Ⅲ.pH=10的NaOH溶液;Ⅳ.pH=10的CH3COONa溶液.(已知常温时醋酸的电离常数为1.75×10-5)
下列有关叙述正确的是 .(忽略溶液混合时的体积变化)
A.Ⅱ、Ⅲ溶液分别与10g铝粉充分反应,生成H2的量Ⅲ一定更多
B.Ⅰ与Ⅱ等体积混合后,溶液中的c(CH3COO-)为原溶液浓度的
C.将Ⅰ和Ⅲ等体积混合后,溶液pH一定小于7
D.四种溶液各10mL分别加水稀释至100mL后,溶液的pH:Ⅲ>Ⅳ>Ⅰ>Ⅱ
(4)常温时某HCl溶液中由水电离出的C(H+)=1×10-amol/L,而相同pH的AlCl3溶液中由水电离出的C(H+)=1×10-bmol/L (已知a,b均为小于14的正整数),则a和b之间满足的关系为 , (用一个等式和一个不等式表示).
查看习题详情和答案>>
①NaHCO3;②NH4HCO3;③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食盐水;⑧CH3COOH; ⑨HCl;=10 ⑩NaOH.
(1)其中属于非电解质的是
(2)NaHCO3溶液显
(3)常温时有四种溶液:Ⅰ.pH=4的CH3COOH溶液;Ⅱ.pH=4的HCl溶液;Ⅲ.pH=10的NaOH溶液;Ⅳ.pH=10的CH3COONa溶液.(已知常温时醋酸的电离常数为1.75×10-5)
下列有关叙述正确的是
A.Ⅱ、Ⅲ溶液分别与10g铝粉充分反应,生成H2的量Ⅲ一定更多
B.Ⅰ与Ⅱ等体积混合后,溶液中的c(CH3COO-)为原溶液浓度的
| 1 | 2 |
C.将Ⅰ和Ⅲ等体积混合后,溶液pH一定小于7
D.四种溶液各10mL分别加水稀释至100mL后,溶液的pH:Ⅲ>Ⅳ>Ⅰ>Ⅱ
(4)常温时某HCl溶液中由水电离出的C(H+)=1×10-amol/L,而相同pH的AlCl3溶液中由水电离出的C(H+)=1×10-bmol/L (已知a,b均为小于14的正整数),则a和b之间满足的关系为