网址:http://m.1010jiajiao.com/timu_id_1730456[举报]
工业制纯碱的第一点是通过饱和食盐水、氨和二氧化碳之间的反应,制取碳酸氢钠晶体。该反应原理可以用以下化学方程式表示,此反应是放热反应。
NH3+CO2+H2O+NaCl(饱和)=== NaHCO3(晶体)↓+NH4Cl
(1)某校学生实验小组利用上述反应原理,设计如图1所示装置,制取碳酸氢钠晶可选用的药品有: a.石灰石b.生石灰c.6mol/L盐酸d.稀硫酸e.浓氨水f.饱和氯化钠溶液。

①A中制备气体时,所需药品是(选填字母代号) ;
②B中盛有饱和碳酸氢钠溶液,其作用是 ;
③在实验过程中,向C中通入气体是有先后顺序的,应先通入气体的化学式为
④检验D出口处是否有氨气逸出的方法是 。
(2)该小组同学为了测定C中所得晶体的碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图2所示实验:

①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是(选填字母序号)
;
A.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
B.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
C.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②操作Ⅲ的方法为 、 、 ;
③所得晶体中碳酸氢钠的纯度为 。
查看习题详情和答案>>工业制纯碱时,第一步是通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠结晶.它的反应原理可以用下面方程式表示:
NH3+CO2+H2O=NH4HCO3
NH4HCO3+NaCl(饱和)=NaHCO3↓+NH4Cl
以上反应总结果是放热反应.请设计一个实验,用最简单的实验装置模拟实现这一过程,获得NaHCO3结晶.可供选择的实验用品有:20%的盐酸、稀硫酸、浓氨水、氢氧化钠、消石灰、石灰石、氯化铵、食盐、蒸馏水、冰,以及中学化学常用仪器.
(1)画出实验装置示意图(包括反应时容器中的物质),并在图中玻璃容器旁自左至右分别用A、B、C、…符号标明.所有仪器的简要画法请见下面的两点说明.

②铁架台、石棉网、酒精灯、玻璃导管之间的联接等,在示意图中不必画出.如需加热,可在需加热的仪器下方标出“△”表示.
(2)写出上图中用A,B,C,…各玻璃容器中盛放的物质的化学式或名称.
(3)利用本题所提供的实验用品,判断得到的产品是碳酸氢钠的结晶,而不是碳酸氢铵或食盐结晶.
查看习题详情和答案>>材料一候氏制纯碱工艺流程图
气体A的饱和溶液
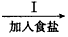 A和食盐的饱和溶液
A和食盐的饱和溶液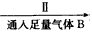 悬浊液
悬浊液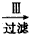 晶体
晶体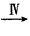 纯碱
纯碱材料二阳离子交换膜法电解饱和食盐水原理示意图

(NH4)2SO4的工艺流程
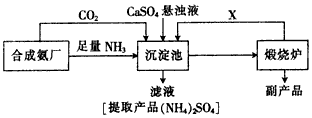
(1)第Ⅳ步操作名称_______,为什么先通入A气体再通B气体?______________。
(2)材料二中精制的食盐水通过离子交换膜电解槽电解,透过阳离子交换膜的离子a是______;b入口通入的溶液是______________,电解饱和食盐水的离子方程式是_____________________。
(3)工业上除用电解法制烧碱外,还可用石灰--纯碱法来生产,写出有关反应方程式:_____________。
(4)材料三中的沉淀池内发生的主要反应方程是______________,从绿色化学和资源综合利用的角度说明上述流程的主要优点是__________________。