摘要:29.2(s)存在饱和溶液中.存在着如下平衡: Mg(OH)2(s) Mg2++2OH-.向该饱和溶液中分别加入固体氯化铵时.固体氢氧化镁的质量减小.在说明原因时.甲.乙两同学存在着明显的分歧. 甲同学认为:氯化铵溶于水.电离出铵根离子.铵根离子发生下列水解: NH4++H2O NH3·H2O+H+.反应产生的氢离子和氢氧化镁反应: Mg(OH)2(s)+2H+ Mg2++2H2O.使Mg(OH)2(s)溶解. 乙同学认为:加入氯化铵固体后.氯化铵溶解并电离.溶液中存在大量的NH4+存在. 2NH4++Mg(OH)2 2NH3·H2O+Mg2+.促进Mg(OH)2溶解. (1)你认为上述解释中 正确.. (2)为了验证上述哪种解释正确.继续做如下实验:在上述氢氧化镁的悬浊液中加入酚酞试液.溶液变红.后逐渐滴加饱和氯化铵溶液.观察溶液颜色的变化和氢氧化镁固体的溶解情况. 若 .说明甲正确. 若 .说明乙正确. (3)常温下.将0.01molNH4C1和0.04molNaOH溶于水.配成0.5L混合溶液.试判断: ①溶液中共有 种粒子. ②溶液中有两种粒子的物质的量之和一定等于0.01mol.它们是 和 . ③溶液中n(OH-)-n(OH4+)-n(H+) mol.
网址:http://m.1010jiajiao.com/timu_id_1730286[举报]
在有固态Mg(OH)2存在的饱和溶液中,存在着如下平衡:
Mg(OH)2(s) ![]() Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq)
向该饱和溶液中分别加入固体NH4Cl时,固体Mg(OH)2的质量有什么变化?_____________________________________________________________________
查看习题详情和答案>>
在有固态Mg(OH)2存在的饱和溶液中,存在着如下平衡:
Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq),向该饱和溶液中分别加入固体CH3COONa、NH4Cl时,固体Mg(OH)2的质量有什么变化?
Mg2+(aq)+2OH-(aq),向该饱和溶液中分别加入固体CH3COONa、NH4Cl时,固体Mg(OH)2的质量有什么变化?
在有固态Mg(OH)2存在的饱和溶液中,存在着如下平衡:
Mg(OH)2(s) Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq)
向该饱和溶液中分别加入固体NH4Cl时,固体Mg(OH)2的质量有什么变化?
在有固态Mg(OH)2存在的饱和溶液中,存在着如下平衡:
Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq)
向该饱和溶液中加入固体NH4Cl时,固体Mg(OH)2的质量有什么变化?
(2012?广东)难溶性杂卤石(K2SO4?MgSO4?2CaSO4?2H2O)属于“呆矿”,在水中存在如下平衡
K2SO4?MgSO4?2CaSO4?2H2O(s)?2Ca2++2K++Mg2++4
+2H2O
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如图1: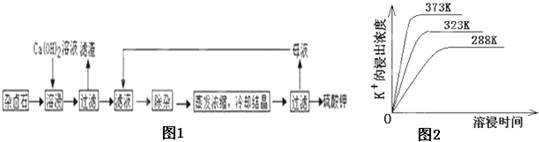
(1)滤渣主要成分有
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
(3)“除杂”环节中,先加入
(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图2,由图可得,随着温度升高,①
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+
?CaCO3(s)+
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K
查看习题详情和答案>>
K2SO4?MgSO4?2CaSO4?2H2O(s)?2Ca2++2K++Mg2++4
| SO | 2- 4 |
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如图1:

(1)滤渣主要成分有
CaSO4
CaSO4
和Mg(OH)2
Mg(OH)2
以及未溶杂卤石.(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
氢氧根与镁离子结合使平衡向右移动,钾离子变多
氢氧根与镁离子结合使平衡向右移动,钾离子变多
.(3)“除杂”环节中,先加入
K2CO3
K2CO3
溶液,经搅拌等操作后,过滤,再加入H2SO4
H2SO4
溶液调滤液PH至中性.(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图2,由图可得,随着温度升高,①
在同一时间K+的浸出浓度大
在同一时间K+的浸出浓度大
②反应速率加快,平衡时溶浸时间短
反应速率加快,平衡时溶浸时间短
;(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+
| CO | 2- 3 |
| SO | 2- 4 |
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K
1.75×104
1.75×104
(计算结果保留三位有效数字).