摘要:22.在一定温度下.容积为1L的密闭容器内.某一反应中M.N的物质的量随反应时间变化的曲线如图.请回答下列问题. (1)该反应的化学方程式为: (2)t1时生成M反应速率 生成N反应速率. (3)达到平衡状态的时间为 .此时N的转化率为 . (4)若生成M反应为吸热反应.在压强不变的情况下升高温度.容器的体积将 .
网址:http://m.1010jiajiao.com/timu_id_1730182[举报]
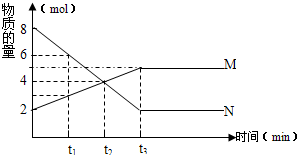 在一定温度下,容积为1L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,
在一定温度下,容积为1L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,请回答下列问题.
(1)该反应的化学方程式为:
2N (g)?M (g)
2N (g)?M (g)
(2)t1时生成M反应速率
大于
大于
(填“大于”“小于”或“等于”)消耗M反应速率(3)达到平衡状态的时间为
t3
t3
(填“t1”“t2”或“t3”),此时N的转化率为75%
75%
.(4)若生成M反应为吸热反应,在压强不变的情况下升高温度、容器的体积将
进行
进行
(填“增大”“减小”或“不变”)在一定温度下,容积为1L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,
请回答下列问题。
(1)该反应的化学方程式为:
(2)t1时生成M反应速率 (填“大于”“小于”或“等于”)消耗M反应速率
(3)达到平衡状态的时间为 (填“t1”“ t2”或“t3”),此时N的转化率为 。
(4)若生成M反应为吸热反应,在压强不变的情况下升高温度、容器的体积将 (填“增大”“减小”或“不变”)

在一定温度下,容积为1L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,
请回答下列问题.
(1)该反应的化学方程式为:______
(2)t1时生成M反应速率______(填“大于”“小于”或“等于”)消耗M反应速率
(3)达到平衡状态的时间为______(填“t1”“t2”或“t3”),此时N的转化率为______.
(4)若生成M反应为吸热反应,在压强不变的情况下升高温度、容器的体积将______(填“增大”“减小”或“不变”)
 查看习题详情和答案>>
查看习题详情和答案>>
请回答下列问题.
(1)该反应的化学方程式为:______
(2)t1时生成M反应速率______(填“大于”“小于”或“等于”)消耗M反应速率
(3)达到平衡状态的时间为______(填“t1”“t2”或“t3”),此时N的转化率为______.
(4)若生成M反应为吸热反应,在压强不变的情况下升高温度、容器的体积将______(填“增大”“减小”或“不变”)
 查看习题详情和答案>>
查看习题详情和答案>>
在1L容积固定的密闭容器中进行A、B、C、D四种气体间的反应,容器内各物质的物质的量随时间的变化如下表:
根据以上信息回答下列问题:
(1)该反应的化学方程式为: ;
(2)反应到第2min时,用B表示的平均反应速率为 mol?L-1?min-1;
(3)反应到第3min时,A物质的转化率为 ;
(4)实验表明升高温度该反应的平衡常数K值会减小,则该反应为 反应(填“放热”或“吸热”),在第4min时改变了某一条件,该条件可能是 ;
A.升温 B.增加B的浓度 C.使用催化剂 D.通入稀有气体
(5)下列能说明该反应达到平衡状态的是 .
A.反应停止了 B.2v(B)消耗=v(C)消耗
C.体系的密度保持不变 D.体系的压强保持不变.
查看习题详情和答案>>
| 时间/物质的量 | n(A)(mol) | n(B)(mol) | n(C)(mol) | n(D)(mol) |
| 起始 | 0.9 | 1.4 | 0 | 0.2 |
| 第1min | 0.6 | 1.1 | 0.15 | |
| 第2min | 0.4 | 0.9 | 0.25 | |
| 第3min | 0.3 | 0.8 | 0.8 | |
| 第4min | 0.3 | 0.8 | 0.3 | 0.8 |
| 第5min | 0.35 | 0.85 | 0.275 | 0.75 |
(1)该反应的化学方程式为:
(2)反应到第2min时,用B表示的平均反应速率为
(3)反应到第3min时,A物质的转化率为
(4)实验表明升高温度该反应的平衡常数K值会减小,则该反应为
A.升温 B.增加B的浓度 C.使用催化剂 D.通入稀有气体
(5)下列能说明该反应达到平衡状态的是
A.反应停止了 B.2v(B)消耗=v(C)消耗
C.体系的密度保持不变 D.体系的压强保持不变.
 (2009?松江区二模)在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
(2009?松江区二模)在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ
测得CO2和CH3OH(g)的浓度随时间变化如图所示:
(1)从反应开始到第10min,氢气的平均反应速率v(H2)=
0.225mol/L?min
0.225mol/L?min
,在这段时间内,反应放出的热量=36.75kJ
36.75kJ
.(2)在该条件下,反应的平衡常数K的值=
5.3
5.3
(保留2位小数),如果在某一时刻保持温度不变,只改变浓度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,则平衡b
b
(填写序号).a.向正反应方向移动 b.向逆反应方向移动
c.不移动 d.无法确定平衡移动方向
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是
cd
cd
(填写序号).a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离 d.再充入1mol CH3OH(g)
(4)在催化剂的作用下,CO2与H2能够合成许多物质,如甲醇.烃类.二甲醚等,但反应体系中混入杂质,则反应很难进行,可能的原因是
催化剂中毒
催化剂中毒
.