网址:http://m.1010jiajiao.com/timu_id_1729907[举报]
下图是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计,其指针总是偏向电源正极。

(1)As(砷)位于元素周期表中第四周期VA族,则Na3AsO4溶液的pH (填“>7”“=7”“<7”=。
(2)向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是 ,D电极上的电极反应式为 。
(3)一段时间后,再向B杯中加入适量的质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置的总的离子方程式为 。
(4)再过一段时间后,G的指针逐渐归零,此时实验装置中的化学反应已经达到化学平衡状态,该反应的化学平衡常数的表达式为:K= 。
查看习题详情和答案>>实验题。已知在常用催化剂(如铂、钯)的催化下,氢气和炔烃加成生成烷烃,难于得到烯烃,但使用活性较低的林德拉催化剂[Pd/(PdO、CaCO3),其中钯附着于碳酸钙及少量氧化铅上],可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化。现有一课外活动兴趣小组利用上述原理设计了一套由如下图所示仪器组装而成的实验装置(铁架台未画出),拟由乙炔制得乙烯,并测定乙炔氢化的转化率。若用含0.020molCaC2的电石和1.60g含杂质18.7%的锌粒(杂质不与酸反应)分别与足量的X和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水VmL。试回答有关问题。
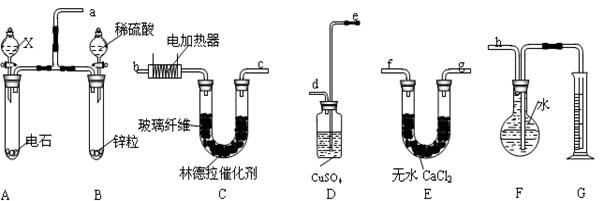 (1)所用装置的连接顺序是a、 、 、 、 、 、 、h(填各接口的字母)。
(1)所用装置的连接顺序是a、 、 、 、 、 、 、h(填各接口的字母)。
(2)写出A中所发生反应的化学方程式(有机物写结构简式): 。
(3)D的作用是___________________。
(4)为减慢A中的反应速率,X应选用____________________________。
(5)F中留下的气体除含少许空气外,还有_______________________________。G所选用的量筒的容积较合理的是______________。
A.500mL B.1000mL C.2000mL
(6)若V=672mL(导管内气体体积忽略不计),则乙炔氢化的转化率为_______________。
查看习题详情和答案>>
B.b电极的周围的颜色变深,说明Fe(OH)3胶粒带有正电
C.Z单质的金属活动性较Cu强
D.装置A、B之间倒置的U型管,是沟通两装置的离子通道

B.b电极的周围的颜色变深,说明Fe(OH)3胶粒带有正电
C.Z单质的金属活动性较Cu强
D.装置A、B之间倒置的U型管,是沟通两装置的离子通道
实验室用如下图所示的装置制取溴化亚铁。(有的装置图未画出)。图中A为CO2发生装置;D和d均盛液溴;E为外套电炉丝的不锈钢管;e是两只耐高温的瓷皿,其中共盛有56g细铁粉。实验开始时先将铁粉加热到600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,最后将d中液溴滴入100℃~200℃的D中。经过几小时的连续反应,在铁管的一端沉积有80g黄绿色鳞片状溴化亚铁。
请回答有关问题:
(1)如何检查用塞子(插有导管和仪器)塞紧的D的气密性?答:________。
(2)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为:________。若在A中盛固体CaCO3,a中盛6mol/L的盐酸,为使导入D中的CO2为干燥纯净的气体,则图中B、C处装置(不必画图)和其中的试剂是:________、________。

(3)实验时,装置D和E的橡胶塞最好用铅箔包住,原因是________。
(4)反应过程中要不断通入CO2,其主要作用是①________;②________。
(5)E中的反应为:2Fe+3![]()
![]() 2
2![]() ,2
,2![]()
![]() 2
2![]() +
+![]() ↑。
↑。
则此实验中溴化亚铁的产率为________。
(6)为防止污染空气,实验时应在F处连接盛________的尾气吸收装置。
查看习题详情和答案>>