网址:http://m.1010jiajiao.com/timu_id_1729870[举报]
(选修—物质结构与性质)(12分)
X、Y、Z三种元素,原子序数依次增大,它们的原子序数之和为43。其中,Y原子的最外层电子数是次外层电子数的三倍。X、Y元素的单质都是构成空气的主要成分。
(1)Z原子的价层电子排布式为____________;XY3-离子的空间构型为__________。
(2)X单质与Y单质直接发生化合反应的化学方程式_________________________。
(3)ZO(氧化物)、FeO晶体结构类型均与NaCl的相同,Z2+和Fe2+离子半径分别为69pm和78pm,则熔点ZO_____ FeO(填“<”或“>” )。
(4)ZO晶体中Z2+的配位数为____________。
(5)化合物A常用于检验Z2+:在稀氨水介质中,A与Z2+
反应可生成鲜红色沉淀,其结构如图所示:
① 该结构中,碳碳之间的共价键类型是______(“σ键”
或“π键”);X与Z2+离子间形成的是配位键,在图
上标出配位键的电子给予的方向。
② 该结构中,Y原子与氢原子除了形成共价键外,
还可存在_______ ;
该结构中,碳原子的杂化轨道类型有_____;Y原子的杂化轨道类型为_____。
查看习题详情和答案>>
【化学-物质结构与性质】(12分)X 、Y 、Z 、W是元素周期表前四周期的4种常见元素,其相关信息如下表:
| 元素 | 相 关 信 息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(1)Y位于元素周期表第 周期 族;Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
(2)XY2是一种常见溶剂,XY2的分子中存在 个σ键。在H-Y、H-Z两种共价键中,键的极性较强的是 (用化学式表示),键长较长的是 (用化学式表示)。
(3)W的基态原子核外电子排布式是 。
W2Y 在空气中煅烧生成 W2O的化学方程式是:
。
(4)处理含 XO 、YO2 烟道气污染的一种方法,是将其在催化剂作用下转化为单质 Y。已知:
XO (g) +1/2O2 (g) = XO2 (g);△H=-283.0kJ/mol
Y (s) +O2 (g) = YO2 (g);△H=-296.0kJ/mol
此反应的热化学方程式是: 。
查看习题详情和答案>>
【化学-物质结构与性质】(12分) X 、Y 、Z 、W是元素周期表前四周期的4种常见元素,其相关信息如下表:
|
元素 |
相 关 信 息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
|
Z |
Z和Y同周期,Z的电负性大于Y |
|
W |
W的一种核素的质量数为63,中子数为34 |
(1)Y位于元素周期表第 周期 族;Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
(2)XY2是一种常见溶剂,XY2的分子中存在 个σ键。在H-Y、H-Z两种共价键中,键的极性较强的是 (用化学式表示),键长较长的是 (用化学式表示)。
(3)W的基态原子核外电子排布式是 。
W2Y 在空气中煅烧生成 W2O 的化学方程式是:
。
(4)处理含 XO 、YO2 烟道气污染的一种方法,是将其在催化剂作用下转化为单质 Y。已知:
XO (g) +1/2O2 (g) = XO2 (g) ;△H=-283.0kJ/mol
Y (s) + O2 (g) = YO2 (g) ;△H=-296.0kJ/mol
此反应的热化学方程式是: 。
查看习题详情和答案>>
【化学-物质结构与性质】(12分)X、Y、Z、W是元素周期表前四周期的4种常见元素,其相关信息如下表:
| 元素 | 相 关 信 息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常见溶剂,XY2的分子中存在 个σ键。在H-Y、H-Z两种共价键中,键的极性较强的是 (用化学式表示),键长较长的是 (用化学式表示)。
(3)W的基态原子核外电子排布式是 。
W2Y在空气中煅烧生成W2O的化学方程式是:
。
(4)处理含XO、YO2 烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。已知:
XO(g)+1/2O2 (g)=XO2 (g);△H=-283.0kJ/mol
Y(s)+O2 (g)=YO2 (g);△H=-296.0kJ/mol
此反应的热化学方程式是: 。 查看习题详情和答案>>
(选修—物质结构与性质)(12分)
X、Y、Z三种元素,原子序数依次增大,它们的原子序数之和为43。其中,Y原子的最外层电子数是次外层电子数的三倍。X、Y元素的单质都是构成空气的主要成分。
(1)Z原子的价层电子排布式为____________;XY3-离子的空间构型为__________。
(2)X单质与Y单质直接发生化合反应的化学方程式_________________________。
(3)ZO(氧化物)、FeO晶体结构类型均与NaCl的相同,Z2+和Fe2+离子半径分别为69pm和78pm,则熔点ZO_____ FeO(填“<”或“>” )。
(4)ZO晶体中Z2+的配位数为____________。
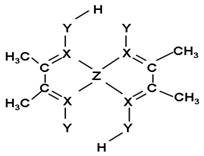
(5)化合物A常用于检验Z2+:在稀氨水介质中,A与Z2+
反应可生成鲜红色沉淀,其结构如图所示:
① 该结构中,碳碳之间的共价键类型是______(“σ键”
或“π键”);X与Z2+离子间形成的是配位键,在图
上标出配位键的电子给予的方向。
② 该结构中,Y原子与氢原子除了形成共价键外,
还可存在_______ ;
该结构中,碳原子的杂化轨道类型有_____;Y原子的杂化轨道类型为_____。
查看习题详情和答案>>