摘要:4.实验室进行中和热的测定的实验装置如下图所示.下列所用的试剂和仪器正确的一组是 A.0.50盐酸.0.50NaOH溶液.100 mL量筒1个 B.0.50盐酸.0.50NaOH溶液.100 mL量筒2个 C.0.50盐酸.0.55NaOH溶液.50 mL量筒1个 D.0.50盐酸.0.55NaOH溶液.50 mL量筒2个
网址:http://m.1010jiajiao.com/timu_id_1729666[举报]
 实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:
实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,则H2SO4 是否剩余
剩余
剩余
,原因是稀H2SO4与Cu不反应,随着反应进行,H2SO4越来越稀,所以H2SO4一定有剩余(
稀H2SO4与Cu不反应,随着反应进行,H2SO4越来越稀,所以H2SO4一定有剩余(
(2)向反应后的溶液中加入足量的CuO,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?xH2O)某小组同学采用加热法测定该晶体里结晶水 x 的值;
①在他们的每次实验操作中至少称量
4
4
次.③加热法测定该晶体里结晶水 x 的值,结晶水完全失去的判断方法是
两次称量不超过0.1g
两次称量不超过0.1g
;④下面是三次实验数据的平均值
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
5.28
5.28
.(3)下列说法正确的是:
bd
bd
(填序号).a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶;
b.KMnO4溶液用于尾气处理;
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生;
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3;
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3.
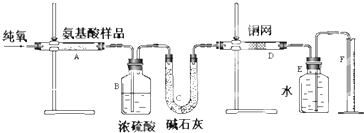
实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成.取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气.现按如图所示装置进行实验:

回答下列问题:
(1)E装置的作用是
(2)需加热的装置是
(3)氨基酸燃烧的化学方程式为
(4)D的作用是
(5)F处读数时应注意的问题是
查看习题详情和答案>>

回答下列问题:
(1)E装置的作用是
排出水,以测量氮气的体积
排出水,以测量氮气的体积
(2)需加热的装置是
A、D
A、D
(填字母).(3)氨基酸燃烧的化学方程式为
CxHyOxNp+(x+
-
)O2
xCO2+
H2O+
N2
| y |
| 4 |
| z |
| 2 |
| 点燃 |
| y |
| 2 |
| p |
| 2 |
CxHyOxNp+(x+
-
)O2
xCO2+
H2O+
N2
| y |
| 4 |
| z |
| 2 |
| 点燃 |
| y |
| 2 |
| p |
| 2 |
(4)D的作用是
吸收未反应的氧气,保证最终收集的是N2
吸收未反应的氧气,保证最终收集的是N2
.(5)F处读数时应注意的问题是
视线应与刻度线和凹液面最低点相切
视线应与刻度线和凹液面最低点相切
. 实验室用50mL 0.50mol?L-1盐酸、50mL 0.55mol?L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
实验室用50mL 0.50mol?L-1盐酸、50mL 0.55mol?L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是
Cu传热快,热量损失大
Cu传热快,热量损失大
.(2)在操作正确的前提下,提高中和热测定准确性的关键是:
提高装置的保温效果
提高装置的保温效果
.(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=
-56.8 kJ?mol-1
-56.8 kJ?mol-1
[盐酸和NaOH溶液的密度按1g?cm-3计算,反应后混合溶液的比热容(c)按4.18J?(g?℃)-1计算].如用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将偏 大
偏 大
(填“偏大”、“偏小”、“不变”).(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是
ABDF
ABDF
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大.
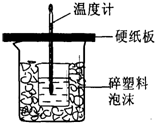 实验室用50mL0.50mol/L盐酸、50mL0.50mol/LNaOH溶液和如图所示装置进行测定中和热的实验,得到表中的数据:
实验室用50mL0.50mol/L盐酸、50mL0.50mol/LNaOH溶液和如图所示装置进行测定中和热的实验,得到表中的数据:| 实验次数 |
起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
环形玻璃搅拌棒
环形玻璃搅拌棒
;实验时用该仪器搅拌溶液的方法是上下搅动
上下搅动
,由图可知该装置有不妥之处,应如何改正?应使小烧杯口与大烧杯口持平,其余部分用碎塑料填满
应使小烧杯口与大烧杯口持平,其余部分用碎塑料填满
.(2)反应需要多次测量温度,每次测量温度后都必须采取的操作是
用水将温度计上的液体冲掉,并擦干温度计
用水将温度计上的液体冲掉,并擦干温度计
.(3)已知Q=cm△t,经数据处理,则该实验测得的中和热△H=
-56.8kJ/mol
-56.8kJ/mol
(盐酸和NaOH溶液的密度按1g/cm3计算,反应后混合溶液的比热容(c)按4.18J/(g?℃)计算).
(4)盐酸与氢氧化钠的中和热的文献值为-57.3kJ/mol,你认为(3)中测得的实验值偏差可能的原因是
①量热计的保温瓶绝热效果不好 ②酸碱溶液混合不迅速
①量热计的保温瓶绝热效果不好 ②酸碱溶液混合不迅速
(至少说出两点)(5)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1
>
>
△H(填“<”、“>”或“=”),理由是NH3?H2O电离吸热
NH3?H2O电离吸热
.