摘要:28.化合物A的结构简式为: 工业上可以最基础的石油产品进行合成.合成A的过程可表示为: 已知:(1) (2) (3) 按要求回答下列问题: (1)写出下列符号所代表物质的结构简式 c: .h: , (2)上述①-⑦的反应中属于取代反应的有 .属于加成反应的有 , (3)A与浓硫酸加热得可B和C.其中B分子中所有碳原子处于同一平面上.则生成B 物质的反应方程式为 .
网址:http://m.1010jiajiao.com/timu_id_1729084[举报]
化合物A的结构简式为 工业上可以最基础的石油产品(乙烯、丙烯、苯等)进行合成。合成A的过程可表示为:
工业上可以最基础的石油产品(乙烯、丙烯、苯等)进行合成。合成A的过程可表示为:
 工业上可以最基础的石油产品(乙烯、丙烯、苯等)进行合成。合成A的过程可表示为:
工业上可以最基础的石油产品(乙烯、丙烯、苯等)进行合成。合成A的过程可表示为:
已知:(1)
(2)
(3)RBr+Mg![]() RMgBr
RMgBr

按要求回答下列问题:
(1)写出下列符号所代表物质的结构简式
c:__________________,h:__________________;
(2)上述①—⑦的反应中属于取代反应的有__________________________,属于加成反应的有_______________________;
(3)A与浓硫酸加热可得B和C,其中B分子中所有碳原子处于同一平面上,则生成B物质的反应方程式为____________________________。
查看习题详情和答案>>《有机化学基础》
(1)有机化学的学习,可以从定性和定量两个角度分析有机物的组成与结构.
①下列有机物中,核磁共振氢谱只有一个吸收峰的是
A.苯 B.甲苯 C.苯酚
②在一定条件下,能发生银镜反应的物质是
A.甲醇 B.乙醛 C.乙酸
③2.3g某常见烃的含氧衍生物完全燃烧,生成4.4g CO2和2.7g H2O有机物.该有机物的分子式为
A.CH4O B.C2H6O C.C2H4O2
(2)某有机化合物的结构如图所示: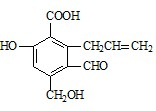
①该有机物能与NaOH发生反应的官能团有:
②1mol该有机物与足量H2发生反应,最多可消耗H2的物质的量为
③该有机物还可以发生的反应为
A.可发生水解反应
B.可发生消去反应
C.与FeCl3溶液发生显色反应
④从分类的角度看,该有机物不可以看作
A.烃类 B.芳香族化合物 C.羧酸类
(3)聚丁二酸乙二醇酯(PES)是一种生物可降解的聚酯,它在塑料薄膜,食品包装和生物材料方面有着广泛的应用.工业上通过以下工艺流程合成PES:
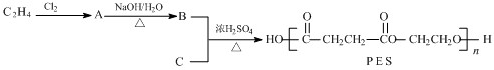
①上述流程中,用于合成A的有机物主要来源于
②写出A→B的化学方程式
③C结构简式是
④有机物A在一定条件下可以发生消去反应,其产物是制造聚氯乙烯塑料的单体.写出A发生的该消去反应的化学方程式
查看习题详情和答案>>
(1)有机化学的学习,可以从定性和定量两个角度分析有机物的组成与结构.
①下列有机物中,核磁共振氢谱只有一个吸收峰的是
A
A
(填字母).A.苯 B.甲苯 C.苯酚
②在一定条件下,能发生银镜反应的物质是
B
B
(填字母)A.甲醇 B.乙醛 C.乙酸
③2.3g某常见烃的含氧衍生物完全燃烧,生成4.4g CO2和2.7g H2O有机物.该有机物的分子式为
B
B
.A.CH4O B.C2H6O C.C2H4O2
(2)某有机化合物的结构如图所示:

①该有机物能与NaOH发生反应的官能团有:
羧基
羧基
、酚羟基
酚羟基
.②1mol该有机物与足量H2发生反应,最多可消耗H2的物质的量为
5
5
mol.③该有机物还可以发生的反应为
C
C
(填字母).A.可发生水解反应
B.可发生消去反应
C.与FeCl3溶液发生显色反应
④从分类的角度看,该有机物不可以看作
A
A
(填字母).A.烃类 B.芳香族化合物 C.羧酸类
(3)聚丁二酸乙二醇酯(PES)是一种生物可降解的聚酯,它在塑料薄膜,食品包装和生物材料方面有着广泛的应用.工业上通过以下工艺流程合成PES:

①上述流程中,用于合成A的有机物主要来源于
石油
石油
.②写出A→B的化学方程式
CH2ClCH2Cl+2H2O
CH2OHCH2OH+2HCl
| NaOH |
CH2ClCH2Cl+2H2O
CH2OHCH2OH+2HCl
.| NaOH |
③C结构简式是
HOOCCH2CH2COOH
HOOCCH2CH2COOH
,B、C通过缩聚
缩聚
反应(填反应类型)制得PES.④有机物A在一定条件下可以发生消去反应,其产物是制造聚氯乙烯塑料的单体.写出A发生的该消去反应的化学方程式
CH2ClCH2Cl
CH2=CHCl+HCl
| NaOH乙醇 |
| △ |
CH2ClCH2Cl
CH2=CHCl+HCl
.| NaOH乙醇 |
| △ |
《有机化学基础》
(1)有机化学的学习,可以从定性和定量两个角度分析有机物的组成与结构.
①下列有机物中,核磁共振氢谱只有一个吸收峰的是 (填字母).
A.苯 B.甲苯 C.苯酚
②在一定条件下,能发生银镜反应的物质是 (填字母)
A.甲醇 B.乙醛 C.乙酸
③2.3g某常见烃的含氧衍生物完全燃烧,生成4.4g CO2和2.7g H2O有机物.该有机物的分子式为 .
A.CH4O B.C2H6O C.C2H4O2
(2)某有机化合物的结构如图所示:
①该有机物能与NaOH发生反应的官能团有: 、 .
②1mol该有机物与足量H2发生反应,最多可消耗H2的物质的量为 mol.
③该有机物还可以发生的反应为 (填字母).
A.可发生水解反应
B.可发生消去反应
C.与FeCl3溶液发生显色反应
④从分类的角度看,该有机物不可以看作 (填字母).
A.烃类 B.芳香族化合物 C.羧酸类
(3)聚丁二酸乙二醇酯(PES)是一种生物可降解的聚酯,它在塑料薄膜,食品包装和生物材料方面有着广泛的应用.工业上通过以下工艺流程合成PES:

①上述流程中,用于合成A的有机物主要来源于 .
②写出A→B的化学方程式 .
③C结构简式是 ,B、C通过 反应(填反应类型)制得PES.
④有机物A在一定条件下可以发生消去反应,其产物是制造聚氯乙烯塑料的单体.写出A发生的该消去反应的化学方程式 . 查看习题详情和答案>>
(1)有机化学的学习,可以从定性和定量两个角度分析有机物的组成与结构.
①下列有机物中,核磁共振氢谱只有一个吸收峰的是 (填字母).
A.苯 B.甲苯 C.苯酚
②在一定条件下,能发生银镜反应的物质是 (填字母)
A.甲醇 B.乙醛 C.乙酸
③2.3g某常见烃的含氧衍生物完全燃烧,生成4.4g CO2和2.7g H2O有机物.该有机物的分子式为 .
A.CH4O B.C2H6O C.C2H4O2
(2)某有机化合物的结构如图所示:

①该有机物能与NaOH发生反应的官能团有: 、 .
②1mol该有机物与足量H2发生反应,最多可消耗H2的物质的量为 mol.
③该有机物还可以发生的反应为 (填字母).
A.可发生水解反应
B.可发生消去反应
C.与FeCl3溶液发生显色反应
④从分类的角度看,该有机物不可以看作 (填字母).
A.烃类 B.芳香族化合物 C.羧酸类
(3)聚丁二酸乙二醇酯(PES)是一种生物可降解的聚酯,它在塑料薄膜,食品包装和生物材料方面有着广泛的应用.工业上通过以下工艺流程合成PES:

①上述流程中,用于合成A的有机物主要来源于 .
②写出A→B的化学方程式 .
③C结构简式是 ,B、C通过 反应(填反应类型)制得PES.
④有机物A在一定条件下可以发生消去反应,其产物是制造聚氯乙烯塑料的单体.写出A发生的该消去反应的化学方程式 . 查看习题详情和答案>>
[化学-有机化学基础]
A、B、C、D四种芳香族化合物有的是药物、有的是香料.它们的结构简式如下所示:

请回答下列问题:
(1)既能使FeCl3溶液显紫色又能和NaHCO3反应放出气体的有______(用A、B、C、D填空).
(2)1molA最多能与______molH2发生加成反应.
(3)B的同分异构体中,苯环上有两个邻位取代基,分别为“-OH”和含有“-COO-”结构的基团共有4种,其中两种(G和H)结构简式如图所示,请补充另外两种.
 ______、______.
______、______.
(4)2006年齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭.D是“亮菌甲素”的结构简式,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.
①写出“亮菌甲素”的分子式______
②核磁共振氢谱分析,发现二甘醇分子中有3个吸收峰,其面积之比为2:2:1;通过质谱法测定它的相对原子质量为106.又知二甘醇中碳、氧元素的质量分数相同,且氢的质量分数为9.43%.1mol二甘醇与足量的金属钠反应生成1molH2.写出二甘醇的结构简式______.
(5)醇和酸在催化剂作用下可直接反应生成酯,而酚不能.酚只能跟有机酸酐作用生成酯.
例如:

现以C为基本原料,请选择必要的其他反应物,用最佳途径合成
请写出其反应的化学方程式:
①______;②______.
查看习题详情和答案>>
A、B、C、D四种芳香族化合物有的是药物、有的是香料.它们的结构简式如下所示:

请回答下列问题:
(1)既能使FeCl3溶液显紫色又能和NaHCO3反应放出气体的有______(用A、B、C、D填空).
(2)1molA最多能与______molH2发生加成反应.
(3)B的同分异构体中,苯环上有两个邻位取代基,分别为“-OH”和含有“-COO-”结构的基团共有4种,其中两种(G和H)结构简式如图所示,请补充另外两种.
 ______、______.
______、______.(4)2006年齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭.D是“亮菌甲素”的结构简式,它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.
①写出“亮菌甲素”的分子式______
②核磁共振氢谱分析,发现二甘醇分子中有3个吸收峰,其面积之比为2:2:1;通过质谱法测定它的相对原子质量为106.又知二甘醇中碳、氧元素的质量分数相同,且氢的质量分数为9.43%.1mol二甘醇与足量的金属钠反应生成1molH2.写出二甘醇的结构简式______.
(5)醇和酸在催化剂作用下可直接反应生成酯,而酚不能.酚只能跟有机酸酐作用生成酯.
例如:

现以C为基本原料,请选择必要的其他反应物,用最佳途径合成

请写出其反应的化学方程式:
①______;②______.
查看习题详情和答案>>
[化学-选修3:物质结构与性质]
硅是重要的半导体材料,构成了现代电子工业的基础.请回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为
(2)硅主要以硅酸盐、
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备.工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是
②SiH4的稳定性小于CH4,更易生成氧化物,原因是
(6)在硅酸盐中,SiO
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式.图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
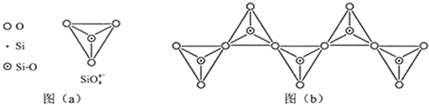
查看习题详情和答案>>
硅是重要的半导体材料,构成了现代电子工业的基础.请回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为
M
M
,该能层具有的原子轨道数为9
9
、电子数为4
4
.(2)硅主要以硅酸盐、
二氧化硅
二氧化硅
等化合物的形式存在于地壳中.(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以
共价键
共价键
相结合,其晶胞中共有8个原子,其中在面心位置贡献3
3
个原子.(4)单质硅可通过甲硅烷(SiH4)分解反应来制备.工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为
Mg2Si+4NH4Cl=SiH4+4NH3+2MgCl2
Mg2Si+4NH4Cl=SiH4+4NH3+2MgCl2
.(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能/(kJ?mol-1) | 356 | 413 | 336 | 226 | 318 | 452 |
C-C键和C-H键较强,所形成的烷烃稳定.而硅烷中Si-Si键和Si-H键的键能较低,易断裂,导致长链硅烷难以生成.
C-C键和C-H键较强,所形成的烷烃稳定.而硅烷中Si-Si键和Si-H键的键能较低,易断裂,导致长链硅烷难以生成.
.②SiH4的稳定性小于CH4,更易生成氧化物,原因是
C-H键的键能大于C-O键,C-H键比C-O键稳定.而Si-H键的键能却远小于Si-O键,所以Si-H键不稳定而倾向于形成稳定性更强的Si-O键
C-H键的键能大于C-O键,C-H键比C-O键稳定.而Si-H键的键能却远小于Si-O键,所以Si-H键不稳定而倾向于形成稳定性更强的Si-O键
.(6)在硅酸盐中,SiO
4- 4 |
sp3
sp3
,Si与O的原子数之比为1:3
1:3
,化学式为SiO32-
SiO32-
.