网址:http://m.1010jiajiao.com/timu_id_1729022[举报]
(08南昌市二模)(16分)某兴趣小组为了验证某种铁的氧化物(FexOy)中含有氧元素并测定其化学式,设计了如下两套实验方案。

方案一,填写下列空白:
(1)按上图连接好各仪器,然后进行的实验操作是 ,接着打开AB之间止水夹,进行的实验操作是 ,再点燃酒精灯。
(2)B中盛放的试剂是 ,能证实铁的化合物中有氧元素存在的实验现象是
(3)写出C中发生的化学反应的化学方程式 。
方案二,填写下列空白
 |
将上述装置的D换成 ,且在C中放入20.3g FexOy粉末(装置气密性良好)
(1)此方案中F的作用是 ;
(2)待C中反应完全后,停止加热,仍然继续通入H2一段时间,其目的是 ;
(3)实验完毕,经称量,发现D增重6.3g,则该铁的氧化物化学式为 。
查看习题详情和答案>>(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+
| A | B |
(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有
(3)某同学要检验Fe3+,向溶液中加入
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
(4)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式
(5)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是
a.铜粉 b.氯气 c.铁粉 d.KSCN溶液.
一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+  Fe3+。在过程A中,Fe2+作 剂。
Fe3+。在过程A中,Fe2+作 剂。
(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有 性。
(3)某同学要检验Fe3+,向溶液中加入 (写化学式)溶液变成红色。要除去FeCl3溶液中少量的氯化亚铁,可行的办法是 (填字母)。
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式 。
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式 。
(5)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是 (填字母)
a.铜粉 b.氯气 c.铁粉 d.KSCN溶液
查看习题详情和答案>>
一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+  Fe3+。在过程A中,Fe2+作 剂。
Fe3+。在过程A中,Fe2+作 剂。
(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有 性。
(3)某同学要检验Fe3+,向溶液中加入 (写化学式)溶液变成红色。要除去FeCl3溶液中少量的氯化亚铁,可行的办法是 (填字母)。
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式 。
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式 。
(5)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是 (填字母)
a.铜粉 b.氯气 c.铁粉 d.KSCN溶液
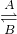 Fe3+.在过程A中,Fe2+作______剂.
Fe3+.在过程A中,Fe2+作______剂.