摘要:21.B. 某研究性学习小组为探究氢氧化钠固体样品中的碳酸钠含量.设计了三种实验方案.请结合以下方案回答有关问题: 方案一:称取一定量的氢氧化钠样品mlg .加水溶解后.逐滴加入沉淀剂至不再产生沉淀为止.将沉淀过滤.洗涤.干燥.称量其质量为 m2g.沉淀剂使用氢氧化钡溶液而不用氢氧化钙溶液.结果将具有更高的精确度.原因是 方案二:利用下图装置测定氢氧化钠样品中 Na2CO3的含量.计算Na2CO3质量分数时.必需测定的数据是 方案三:操作流程如下: 需直接测定的数据是 ,在转移溶液时.如溶液转移不完全.则Na2CO3质量分数的测定结果 (填“偏大 .“偏小 或“不变 ).
网址:http://m.1010jiajiao.com/timu_id_1728494[举报]
某研究性学习小组为了探究镁粉与溴水反应的机理,做了如下四组实验:①将镁粉投入冷水中,未见任何现象;②将镁粉放入溴水中,观察到只是开始时产生极少量的气泡,但溴水的颜色逐渐褪去;③将镁粉放入液溴中,未观察到任何明显现象;④向含足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快褪去.则下列关于镁与溴水的反应机理的论述中正确的是( )
查看习题详情和答案>>
 某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定该实验条件下的气体摩尔体积,设计的简易实验装置如图.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定该实验条件下的气体摩尔体积,设计的简易实验装置如图.该实验的主要操作步骤如下:①配制浓度均为1mol/L的盐酸和醋酸溶液;
②用
酸式滴定管
酸式滴定管
量取10.00mL 1mol/L的盐酸和醋酸溶液分别加入两个锥形瓶中;③分别称取除去表面氧化膜的镁带a g,并系于铜丝末端,a的数值至少为
0.12
0.12
;④在广口瓶中装足量的水,按图连接好装置;检查装置的气密性;
⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不与酸接触),至反应完全,记录
反应所需时间
反应所需时间
;⑥反应结束后待温度恢复到室温,若丙中液面高于乙中液面,读取量筒中水的体积前,应
将量筒缓缓向下移动,使乙、丙中液面相平
将量筒缓缓向下移动,使乙、丙中液面相平
,读出量筒中水的体积为V mL.请将上述步骤补充完整并回答下列问题:
(1)用文字表述④检查该装置气密性的操作与观察方法:
往丙中加水没过导气管口下端,两手掌紧贴甲外壁一会儿,若观察到丙中导气管冒气泡,表明装置不漏气;
往丙中加水没过导气管口下端,两手掌紧贴甲外壁一会儿,若观察到丙中导气管冒气泡,表明装置不漏气;
.(2)本实验中应选用
B
B
(填序号)的量筒.A.100mL B.200mL C.500mL
(3)若水蒸气的影响忽略不计,在实验室条件下,气体摩尔体积的计算式为Vm=
0.2VL/mol
0.2VL/mol
.(4)速率不等的原因是
H+浓度不同
H+浓度不同
,铜丝不与酸接触的原因是防止形成原电池,加快反应速率,干扰实验测定;
防止形成原电池,加快反应速率,干扰实验测定;
. 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH3CH-CH2+CO+H2
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH3CH-CH2+CO+H2| 一定条件 |
| H2 |
| Ni,△ |
| 浓H2SO4 |
| △ |
请填写下列空白:
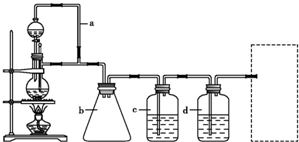
(1)写出实验室制备氢气的化学方程式:
(2)若用以上装置制备干燥纯净的CO,装置中b的作用分别是
(3)制丙烯时,还产生少量SO2,CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是
①足量饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④无水CuSO4 ⑤品红溶液
(4)如图所示装置工作时均与H2有关.
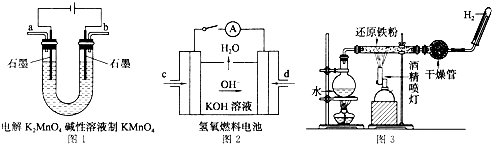
①图1所示装置中阳极的电极反应式为
②图2所示装置中,通入H2的管口是
③某同学按图3所示装置进行实验,实验结束后,将玻璃管内固体物质冷却后,溶于稀硫酸,充分反应后,滴加KSCN溶液,溶液不变红,再滴入新制氯水,溶液变为红色.该同学据此得出结论:铁与水蒸气反应生成FeO和H2.该结论
某研究性学习小组为研究氯气是否具有漂白性,设计如下实验装置.试根据实验装置回答下列问题:

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液
(1)在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的 .
(2)B中的液体为 ,其作用为 .
(3)A、C中有色布条的颜色变化分别为 ,A、C的实 验现象说明氯气是否具有漂白性? (填“是”或“否”).
(4)D中NaOH溶液的作用 (用离子方程式说明).
(5)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去.组内有甲、乙两种 意见:
甲:氯气溶于水溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色.
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则 的意见正确.(填“甲”或“乙”)
查看习题详情和答案>>

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液
(1)在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的
(2)B中的液体为
(3)A、C中有色布条的颜色变化分别为
(4)D中NaOH溶液的作用
(5)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去.组内有甲、乙两种 意见:
甲:氯气溶于水溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色.
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则
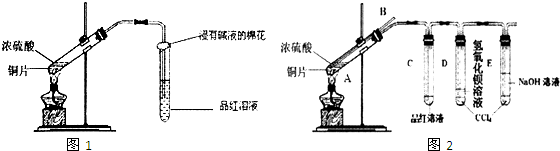
某研究性学习小组为探究Cu与浓H2SO4的反应及其产物SO2的性质,设计如图1实验装置:
(1)写出铜与浓硫酸反应的化学方程式: ;浸有碱液的棉花的作用是 .
(2)该小组同学在实验中发现以上实验装置有相当多不足之处,如实验不够安全和易造成环境污染等.为改进实验和更多地了解SO2的性质,经过同学问的讨论和与老师的交流,设计了如图2实验装置.
①请写出长导管B的作用 (只写一点就可).
②对试管A中的浓H2SO4和铜片进行加热,发现E试管中有气泡逸出,品红溶液很快褪色,但最终未见D试管中氢氧化钡溶液出现浑浊.为探究D试管中未出现浑浊的原因,该小组同学在化学手册中只查阅到下列物质常温下的溶解度数据:
请你应用类比研究方法帮他们预测D试管未出现浑浊的原因: .
③为验证D试管中溶液的组成,进行了下列实验,请你帮他们完成下列实验内容:
 查看习题详情和答案>>
查看习题详情和答案>>
(1)写出铜与浓硫酸反应的化学方程式:
(2)该小组同学在实验中发现以上实验装置有相当多不足之处,如实验不够安全和易造成环境污染等.为改进实验和更多地了解SO2的性质,经过同学问的讨论和与老师的交流,设计了如图2实验装置.
①请写出长导管B的作用
②对试管A中的浓H2SO4和铜片进行加热,发现E试管中有气泡逸出,品红溶液很快褪色,但最终未见D试管中氢氧化钡溶液出现浑浊.为探究D试管中未出现浑浊的原因,该小组同学在化学手册中只查阅到下列物质常温下的溶解度数据:
| 物质 | 溶解度(g/100水) | 物质 | 溶解度(g/100水) |
| Ca(OH)2 | 0.173 | Ba(OH)2 | 3.89 |
| CaCO3 | 0.0013 | BaSO3 | 0.016 |
| Ca(HCO3)2 | 16.60 |
③为验证D试管中溶液的组成,进行了下列实验,请你帮他们完成下列实验内容:
| 实验方案 | 现象 |
| 1.取少量溶液于试管中,加入稀盐酸,加热, 用湿润的蓝色石蕊试纸检验生成的气体. |
|
| 2.取少量溶液于试管中,加入 |
 查看习题详情和答案>>
查看习题详情和答案>>