摘要:21. 高温 硫酸是工业生产中一种重要的化工产品.我国工业生产硫酸的主要方法是接触法.主要原料为黄铁矿.请回答下列问题: (1)已知煅烧黄铁矿的化学方程式为 4FeS2 + 11O2 2Fe2O3 + 8SO2 该反应中氧化剂和氧化产物之比为 ,标准状态下得到4.48升SO2 时.一共转移了 mole- . (2)已知温度.压强对SO2平衡转化率的影响如下表所示: 压强 / MPa 转化率 / % 温度 / ℃ 0.1 0.5 1 10 400 99.2 99.6 99.7 99.9 500 93.5 96.9 97.8 99.3 600 73.7 85.8 89.5 96.4 根据上表回答.SO2转化到SO3的最佳反应条件是 . A.400-500℃ 0.1 MPa B.400℃ 10 MPa C.500℃ 10 MPa D.400-500℃ 1 MPa (3)在一定条件下.1mol SO2完全转化成SO3气体时放出热量为Q1 KJ.写出该反应的热化学方程式: .若在该条件下将2 mol SO2 放入一定容积的密闭容器中.一段时间后测得反应放出热量为Q2 KJ.则此时SO2的转化率为 (用含Q1.Q2代数式表示). (4)市售浓硫酸的密度是1.84 g / cm3.质量分数为98 % .若用H2SO4· XH2O来表示这种浓硫酸.则X为 .
网址:http://m.1010jiajiao.com/timu_id_1728153[举报]
硫酸是工业生产中一种重要的化工产品,我国工业生产硫酸的主要方法是接触法,主要原料为黄铁矿,请回答下列问题:
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+11O2
2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:
根据上表回答,SO2转化到SO3的最佳反应条件是
A.400-500℃0.1MPa B.400℃10MPa
C.500℃10MPa D.400-500℃1MPa
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 KJ,写出该反应的热化学方程式:
%
% (用含Q1、Q2代数式表示).
(4)市售浓硫酸的密度是1.84g/cm3、质量分数为98%,若用H2SO4?XH2O来表示这种浓硫酸,则X为
.
查看习题详情和答案>>
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+11O2
| ||
11:10
11:10
;标准状态下得到4.48升SO2时,一共转移了1.1
1.1
mole-.(2)已知温度、压强对SO2平衡转化率的影响如下表所示:
压强/MPa 转化率/% 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
A
A
.A.400-500℃0.1MPa B.400℃10MPa
C.500℃10MPa D.400-500℃1MPa
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 KJ,写出该反应的热化学方程式:
2SO2(g)+O2(g) 2SO3(g)△H=-2Q1 KJ/mol或SO2(g)+
2SO3(g)△H=-2Q1 KJ/mol或SO2(g)+
O2(g) SO3(g)△H=-Q1 KJ/mol
SO3(g)△H=-Q1 KJ/mol
 2SO3(g)△H=-2Q1 KJ/mol或SO2(g)+
2SO3(g)△H=-2Q1 KJ/mol或SO2(g)+| 1 |
| 2 |
 SO3(g)△H=-Q1 KJ/mol
SO3(g)△H=-Q1 KJ/mol2SO2(g)+O2(g) 2SO3(g)△H=-2Q1 KJ/mol或SO2(g)+
2SO3(g)△H=-2Q1 KJ/mol或SO2(g)+
O2(g) SO3(g)△H=-Q1 KJ/mol
SO3(g)△H=-Q1 KJ/mol
.若在该条件下将2mol SO2 放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 KJ,则此时SO2的转化率为 2SO3(g)△H=-2Q1 KJ/mol或SO2(g)+
2SO3(g)△H=-2Q1 KJ/mol或SO2(g)+| 1 |
| 2 |
 SO3(g)△H=-Q1 KJ/mol
SO3(g)△H=-Q1 KJ/mol| 50Q2 |
| Q1 |
| 50Q2 |
| Q1 |
(4)市售浓硫酸的密度是1.84g/cm3、质量分数为98%,若用H2SO4?XH2O来表示这种浓硫酸,则X为
| 1 |
| 9 |
| 1 |
| 9 |
氨是一种重要的化工产品,是氮肥工业及制造硝酸的原料.为探究氨气的性质,某研究性学习小组做了以下实验:
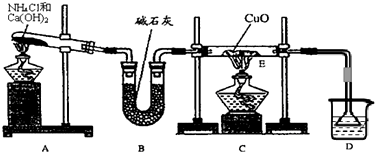
(1)实验室用A图所示实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物来制取氨气.
①实验室制取氨气的化学方程式为 .
②若用加热碳酸氢铵固体制取纯净的氨气,你认为装置中U型管的作用是 .
(2)在实验中发现E装置中的固体由黑色变为红色,可推测氨气具有 性.
(3)某同学查阅资料发现Cu2O粉末也呈红色,因此推测上述红色固体中可能还含有Cu2O.已知:①Cu2O是碱性氧化物,在酸性溶液中Cu+不稳定,易转化为Cu和Cu2+.
②在空气中高温灼烧时:Cu2O稳定、不分解,而CuO将分解生成Cu2O和O2.
现有浓硝酸、稀硫酸、稀硝酸、氢氧化钠溶液及pH试纸,而没有其他试剂,请用最简便的实验方法证明红色固体中是否含有Cu2O.(简述操作方法、现象和结论)
(4)现有一份一定质量Cu和Cu2O混合物,向其中加入0.4L 3.0mol/L稀硝酸,混合物完全溶解,同时生成4.48L NO(标准状况),向所得溶液中加入一定体积1.0mol/L NaOH溶液恰好使Cu2+沉淀完全,沉淀经洗涤、充分灼烧可得32.0g固体.下列有关说法正确的是【已知:3Cu2O+14HNO3(稀)═6Cu(NO3)2+2NO↑+7H2O】 :
A.加入NaOH溶液的体积为1.2L
B.Cu和Cu2O混合物质量为27.2g
C.混合物完全溶解后溶液中n(H+)=0.3mol
D.将等质量混合物完全还原至少需标准状况下H21.12L. 查看习题详情和答案>>

(1)实验室用A图所示实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物来制取氨气.
①实验室制取氨气的化学方程式为
②若用加热碳酸氢铵固体制取纯净的氨气,你认为装置中U型管的作用是
(2)在实验中发现E装置中的固体由黑色变为红色,可推测氨气具有
(3)某同学查阅资料发现Cu2O粉末也呈红色,因此推测上述红色固体中可能还含有Cu2O.已知:①Cu2O是碱性氧化物,在酸性溶液中Cu+不稳定,易转化为Cu和Cu2+.
②在空气中高温灼烧时:Cu2O稳定、不分解,而CuO将分解生成Cu2O和O2.
现有浓硝酸、稀硫酸、稀硝酸、氢氧化钠溶液及pH试纸,而没有其他试剂,请用最简便的实验方法证明红色固体中是否含有Cu2O.(简述操作方法、现象和结论)
(4)现有一份一定质量Cu和Cu2O混合物,向其中加入0.4L 3.0mol/L稀硝酸,混合物完全溶解,同时生成4.48L NO(标准状况),向所得溶液中加入一定体积1.0mol/L NaOH溶液恰好使Cu2+沉淀完全,沉淀经洗涤、充分灼烧可得32.0g固体.下列有关说法正确的是【已知:3Cu2O+14HNO3(稀)═6Cu(NO3)2+2NO↑+7H2O】
A.加入NaOH溶液的体积为1.2L
B.Cu和Cu2O混合物质量为27.2g
C.混合物完全溶解后溶液中n(H+)=0.3mol
D.将等质量混合物完全还原至少需标准状况下H21.12L. 查看习题详情和答案>>
氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色.已知pH为5时,+2价铜已开始以碱式盐的形式沉淀.某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示了处理废料的综合利用方案:

(1)加入的A是
(2)反应②的离子方程式是
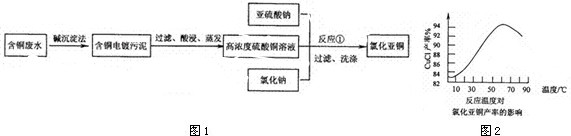
(3)保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如图二所示.则溶液温度控制在
查看习题详情和答案>>

(1)加入的A是
稀硫酸
稀硫酸
,通入的B是空气
空气
.(2)反应②的离子方程式是
2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO4-+2H+
2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO4-+2H+
.为提高Cu2Cl2的产率,常在反应②的溶液中加适量稀碱溶液,控制pH为3.5.这样做的目的是OH-中和了反应生成的H+,有利于反应向右进行,提高Cu2Cl2的产率
但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
OH-中和了反应生成的H+,有利于反应向右进行,提高Cu2Cl2的产率
但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
.但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
(3)保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如图二所示.则溶液温度控制在
53℃~55℃
53℃~55℃
时,Cu2Cl2的产率已达到94%,当温度高于65℃时,Cu2Cl2产率会下降,其原因可能是温度过高,促进了CuCl2的水解
温度过高,促进了CuCl2的水解
.
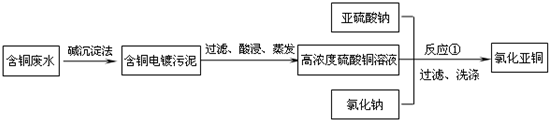
 氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色.以下是一种采用亚硫酸盐还原法,从含铜电镀废水中制备氯化亚铜的工艺流程图.请回答以下问题:
氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色.以下是一种采用亚硫酸盐还原法,从含铜电镀废水中制备氯化亚铜的工艺流程图.请回答以下问题: