网址:http://m.1010jiajiao.com/timu_id_1727738[举报]
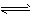 2HCrO4-
2HCrO4- 2H++2CrO42- ,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
2H++2CrO42- ,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为 B. Ag2CrO4
C. AgHCrO4
D. Ag2O
(1)请完成并配平如下的化学方程式(将未知物的化学式和化学计量数填入)
(2)浓盐酸在上述反应中显示(填写序号)
A.只有还原性 B.只有氧化性 C.只有酸性 D.既有氧化性又有还原性 E.既有酸性又有还原性
(3)若反应中转移0.6mol 电子,则被氧化的还原剂的物质的量为
(4)已知ClO2(气体)具有很强的氧化性,故常用作消毒剂,其消毒的效率(以单位质量的消毒剂得到电子的物质的量大小来表示) 约是Cl2的
(分)高铁酸钾是一种重要的水的处理剂,实验可用下列流程制取高铁酸钾,

⑴NaClO溶液中加入NaOH固体形成碱性环境。
⑵将研磨的Fe(NO3)3 少量多次的加入到上述溶液中,冰浴中反应1h。
采用少量多次加入,其目的是___________________________;该反应的离子方程为:
_____________________________________。
⑶将KOH加入到反应后的溶液搅拌半小时。静置,抽滤的粗产品。该反应的化学方程式为:_____________________________。
⑷依次用甲苯、乙醇、乙醚洗涤以除去水份和KNO3、KCl、KOH等杂质。
⑸在强碱性溶液中,高铁酸钾能将亚铬酸盐(KCrO2)氧化为铬酸盐(K2CrO4),生成的铬酸盐溶液酸化后,得到的重铬酸钾(K2Cr2O7)用Fe(Ⅱ)的标准溶液滴定,以二苯胺磺酸钠为指示剂。到达滴定终点时,溶液由紫色变为淡绿色。现称取5.000 g高铁酸钾样品于烧杯中,加入适量氢氧化钾溶液,加入稍过量的KCrO2,充分反应后,转移到250 mL容量瓶中,定容,量取25.00mL,再用稀硫酸酸化,用0.1000 mol·L-1的(NH4)2Fe(SO4)2标准溶液滴定,用去标准溶液33.33 mL。
①滴定时适宜选用的滴定管是: (a、酸式,b、碱式)。
②计算上述实验制得的样品中,高铁酸钾的质量分数为_________________。
③若上述过程中,测得的样品中高铁酸盐的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有__________ 。
查看习题详情和答案>>浓盐酸与重铬酸钾[K2Cr2O7(s)]共热时产生某种气体单质X,产物中还有三氯化铬等生成。这种方法制X时便于控制反应,撤去酒精灯则反应停止。现在要制得纯净的X(装置如图)。

(1)加热时,a与b反应的化学方程式__________________________________
(2)液体C的作用是_____________________________________________
现在把制得的纯净干燥的X通入下图所示的装置。

(3)e是FeBr2溶液,一段时间后观察到的实验现X象是________________________________
(4)f是浸有一种钾盐溶液的棉球,一段时同后观察到试管内有紫色气体,则大试管内发生反应的化学方程式为________________________
(5)g是水和CCl4的混合物,可看到颜色较深的液体在____ (填“上”或“下”)层.
(6)h是碱石灰,则此装置的作用是______________________________________________
查看习题详情和答案>>