摘要:22.16mL由NO与NH3组成的混合气体在催化剂作用下于400℃左右发生如下反应: 6NO(g)+4NH3(g) 5N2(g)+6H2O(g).达平衡后在相同条件下混合气体的体积烃为17mL.原混合气体中 NO与NH3的物质的量之比可能是 ( ) ①3:1 ②3:2 ③3:4 ④3:5 A.①② B.①④ C.②③ D.③④
网址:http://m.1010jiajiao.com/timu_id_1727558[举报]
1.6 mol由NO和NH3组成的混合气体,在催化剂作用下于400 ℃ 左右可发生6NO+4NH3 5N2+6H2O,达到平衡后,在相同条件下混合气体的物质的量变为1.7 mol。则被氧化N的物质的量为
5N2+6H2O,达到平衡后,在相同条件下混合气体的物质的量变为1.7 mol。则被氧化N的物质的量为
 运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.
运用化学反应原理研究氮、硫、氯等单质及其化合物的反应有重要的意义.(1)放热反应2SO2(g)+O2(g)=2SO3(g)是硫酸工业上的重要反应,在体积不变的条件下,下列措施有利于提高SO2平衡转化率的有
A、升高温度 B、降低温度 C、减小压强 D、加入催化剂 E.移出氧气
(2)氮是大气中含量最多的一种元素,氮及其化合物在工农业生产、生活中有着重要应用.用CH4将氮氧化物(用NOx表示)催化还原为N2可以消除氮氧化物带来的污染,该反应的化学方程式为
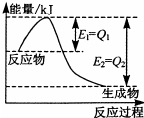
(3)如图是一定的温度和压强下,N2和H2反应生成1mol NH3过程中的能量变化图,请写出工业合成氨的热化学方程式
(4)在25℃下,将xmol/L的氨水与y mol/L的盐酸等体积混合,反应后溶液显中性,则c(NH4+ )
(5)已知:25℃时,Ksp(AgCl)=1.8×10-10、Ksp(AgBr)=4.9×10 -13.现在向0.001mol/L KBr和0.01mol/L KCl混合溶液中滴加0.1mol/L AgNO3溶液(反应过程中溶液体积变化忽略不计),当出现AgCl沉淀时.c(Br-)=