摘要:14.将amolCu2S与cmol/LbL的硝酸恰好反应.生成硝酸铜.硫酸.一氧化氮.水.则参加反应的硝酸中.未被还原的硝酸的物质的量为 ( ) ①4amol ②6amol ③amol ④amol A.①② B.②③ C.①④ D.③④ 卷Ⅱ
网址:http://m.1010jiajiao.com/timu_id_1727343[举报]
实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气.供选用的实验试剂及装置如下(部分导管、蒸馏水略):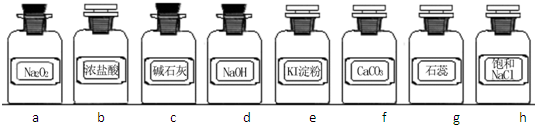
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式 .
(2)下列装置组合最合理的是 (填序号,需考虑实验结束撤除装置时残留有害气体的处理).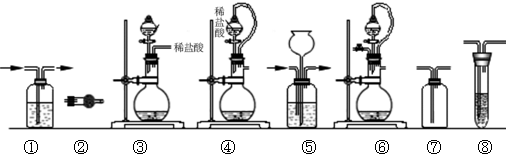
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为: .
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
① ,
② .
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一? (填“是”或“否”);
理由是 .
查看习题详情和答案>>

(1)写出用Na2O2与浓盐酸制备氯气的化学方程式
(2)下列装置组合最合理的是

| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③、⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ④、⑥ | ⑤ | ⑧/g | ① |
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①
②
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?
理由是
MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果.某兴趣小组通过实验研究MnO2性质.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是
A.把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2溶液,观察是否有白色沉淀生成
D.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比实验:
①该小组从上述对比实验中,可以得出的结论是
②写出在酸性条件下MnO2氧化I-的离子方程式
(3)为了探究MnO2的催化效果,需要用30%的H2O2溶液(密度按1g/cm3)配制浓度为3%的H2O2溶液(密度按1g/cm3)100mL.配制过程中除了用到量筒、烧杯、100mL容量瓶外,还需用到的玻璃仪器名称是
(4)实验室用MnO2制取氯气的化学方程式为
查看习题详情和答案>>
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是
A
A
.A.把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2溶液,观察是否有白色沉淀生成
D.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比实验:
| 实验 | 外加试剂 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸 | 迅速变棕褐色 |
酸性越强,MnO2氧化性越强
酸性越强,MnO2氧化性越强
.②写出在酸性条件下MnO2氧化I-的离子方程式
2I-+MnO2+4H+═I2+Mn2++2H2O
2I-+MnO2+4H+═I2+Mn2++2H2O
.(3)为了探究MnO2的催化效果,需要用30%的H2O2溶液(密度按1g/cm3)配制浓度为3%的H2O2溶液(密度按1g/cm3)100mL.配制过程中除了用到量筒、烧杯、100mL容量瓶外,还需用到的玻璃仪器名称是
玻璃棒、胶头滴管
玻璃棒、胶头滴管
,需用量筒量取10.0
10.0
mL30%的H2O2溶液.MnO2催化H2O2分解的化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,反应结束后将液体与MnO2分离的实验操作名称叫
| ||
过滤
过滤
.(4)实验室用MnO2制取氯气的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2 ↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2 ↑+2H2O
.
| ||
为了避免青铜器生成铜绿,以下方法正确的是( )
| A、将青铜器放在银质托盘上 | B、将青铜器与直流电源的正极相连 | C、将青铜器保存在潮湿的空气中 | D、在青铜器的表面覆盖一层防渗的高分子膜 |