摘要:17.常温下在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/ L HC1溶液40mL.溶液的PH值逐渐降低.此时溶液中含碳元素的微粒物质的量浓度的百分含量也发生变化(CO2因逸出未画出).如下图所示 回答下列问题: (1)在0.1mol/L Na2CO3溶液所有阳离子和阴离子的浓度有何关系? . (2)当加入盐酸使溶液PH值为10时.混合液中含碳元素的离子物质的量之比为 . (3)随着盐酸的加入.请写出BC段的离子方程式 . (4)当混合液的PH= 时.开始放出CO2气体.
网址:http://m.1010jiajiao.com/timu_id_1727298[举报]
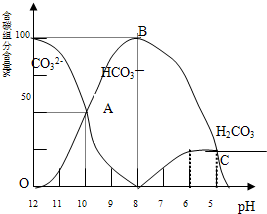 常温下在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示:回答下列问题:
常温下在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示:回答下列问题:(1)20mL 0.1mol/LNa2CO3溶液呈碱性的原因是(用离子方程式表示)
(2)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32-离子不超过其总量的10%.请你设计简单实验证明该同学的观点是否正确
(3)若向20mL 0.1mol/LNa2CO3溶液中加入BaCl2粉末3.328×10-7g时开始产生沉淀X,则Ksp(X)=
(4)请写出OAB段的离子方程式
常温下在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/ L HC1溶液40mL,溶液的PH值逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如下图所示回答下列问题:
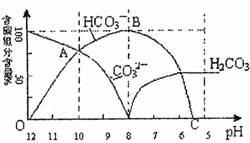
(1) 在0.1mol/L Na2CO3溶液所有阳离子和阴离子的浓度有何关系?(用等式表示)
。
(2)当加入盐酸使溶液PH值为10时,混合液中含碳元素的离子物质的量之比为 。
(3)随着盐酸的加入,请写出BC段的离子方程式 。
(4)当混合液的PH= 时,开始放出CO2气体。
查看习题详情和答案>>常温下在20mL 0.1mol.L-1 Na2CO3溶液中逐渐加入0.1mol.L-1的HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒的物质的量的百分量(纵轴)也发生变化(CO2会逸出未画出),如图所示,回答下列问题:
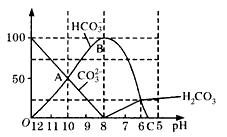
(1)随着盐酸的加入,HCO3-的浓度变化趋势是____;请写出 OAB段的离子方程式:____。
(2)当加入盐酸使溶液的pH=10时,混合溶液中含碳元素的离子有 ____,其物质的量之比是____;当pH=7时,混合溶液中含碳元素的微粒有____。
(3)在pH=____时开始逸出CO2气体,当pH=5时,逸出的气体的物质的量____0. 002mol(填“>”、“<”或“=”)。
查看习题详情和答案>>
(2)当加入盐酸使溶液的pH=10时,混合溶液中含碳元素的离子有 ____,其物质的量之比是____;当pH=7时,混合溶液中含碳元素的微粒有____。
(3)在pH=____时开始逸出CO2气体,当pH=5时,逸出的气体的物质的量____0. 002mol(填“>”、“<”或“=”)。