摘要:23.往稀硫酸和稀盐酸的混合液50ml中加入粉末2.1375g.充分反应后.沉淀经干燥为1.165g.所得溶液pH为13.则原混合溶液中硫酸和稀盐酸的物质的量浓度为多少?(假定反应前后溶液体积不变)
网址:http://m.1010jiajiao.com/timu_id_1727163[举报]
稀硫酸和稀盐酸的混合液50 mL,加入氢氧化钡粉末2.1375 g,充分反应后过滤,得干燥沉淀1.165 g,所得溶液的pH值为13。原混合溶液中SO42- 和Cl-的物质的量浓度分别是多少?
查看习题详情和答案>>稀硫酸和稀盐酸的混合液100 mL,加入氢氧化钡粉末3.42g,充分反应后过滤,得干燥沉淀2.33g,所得溶液的pH值为13(假设溶液仍为100 mL)。求原混合溶液中盐酸的物质的量浓度是少?
查看习题详情和答案>>有一种白色粉末,可能含有下列阴离子和阳离子中的几种,阴离子:S2-、Cl-、NO
、SO
、CO
、HCO
、MnO
.阳离子:Na+、Mg2+、Al3+、Ba2+、Fe2+、Fe3+、Cu2+、NH
.现将该白色粉末进行下列实验:
续表
根据实验推断:(白色沉淀不溶于稀HN0?)
(1)从a实验中,可推断粉末中不可能有 ;
(2)从b实验中,可推断粉末中不可能有 ;
(3)从c实验中,可推断粉末中不可能有 ;
(4)从d实验中,可推断粉末中不可能有 ,必定含有 ;
(5)综上所述,粉末中还可能含有 .
查看习题详情和答案>>
- 3 |
2- 4 |
2- 3 |
- 3 |
- 4 |
+ 4 |
| 实验操作 | 现象 |
| a、取少量粉末,加水、振荡 | 全部溶解、溶液无色透明 |
| b、向所得溶液中慢慢滴入NaOH溶液并加热 | 无明显现象 |
| 实验操作 | 现象 |
| c、取少量粉末,加盐酸 | 无明显现象 |
| b、取少量粉末,加稀BaCl2和稀盐酸的混合液 | 有白色沉淀生成 |
(1)从a实验中,可推断粉末中不可能有
(2)从b实验中,可推断粉末中不可能有
(3)从c实验中,可推断粉末中不可能有
(4)从d实验中,可推断粉末中不可能有
(5)综上所述,粉末中还可能含有
 实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55℃~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:
实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55℃~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:| 熔点 | 沸点 | 状态 | |
| 苯 | 5.51℃ | 80.1℃ | 液体 |
| 硝基苯 | 5.7℃ | 210.9℃ | 液体 |
将浓H2SO4沿烧杯内壁缓缓注入浓HNO3中,并用玻璃棒不断搅拌
将浓H2SO4沿烧杯内壁缓缓注入浓HNO3中,并用玻璃棒不断搅拌
.(2)分离硝基苯和水的混合物的方法是
分液
分液
;分离硝基苯和苯的方法是蒸馏
蒸馏
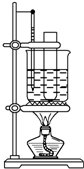
.(3)某同学用如图装置制取硝基苯:
①用水浴加热的优点是
使反应体系受热均匀,容易控制温度
使反应体系受热均匀,容易控制温度
;②指出该装置的两处缺陷
试管底部不能与烧杯底部接触
试管底部不能与烧杯底部接触
;缺少一个带有长直玻璃导管的橡皮塞
缺少一个带有长直玻璃导管的橡皮塞
.