网址:http://m.1010jiajiao.com/timu_id_1727128[举报]
欲测定在干燥空气中已部分氧化的Na2SO3样品中Na2SO3的质量分数,甲、乙两组分别设计并完成实验如下:
甲组:称取ag样品,利用下图(甲)所示装置(B、C之间导管先充满水),测出A中加入足量较浓H2SO4反应后,量筒C中水的体积V mL。


(1)B、C之间导管先充满水的目的 。
(2)你认为本组实验的Na2SO3测定值将偏 (填“高”或“低”),主要原因是 。
(3)简述最简单改进的方法 。
乙组:称取a g样品,利用图(乙)所示装置,测出A中加入足量较浓H2SO4后装置C中足量碱石灰增重为b g。
(1)B装置的作用是 ,
D装置的作用是 。
(2)你认为本组实验的Na2SO3测定值将偏 (高、低),主要原因是
。
查看习题详情和答案>>长期存放在Na2SO3会被空气中的氧气部分氧化。某化学兴趣小组通过实验测不定期某无水Na2SO3被氧化的程度。
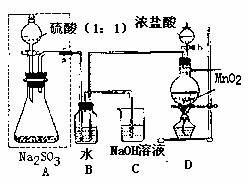
请回答:
(1)若将虚线框内的分液漏斗换成长颈漏斗,是应如何检查虚线框内装置的气密性?
。
(2)写出B装置中反应的离子方程式 。
(3)称量a g Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量BaC12溶液充分反应,过滤、洗涤、干燥、称量得白色沉淀b g,则样品中的Na2SO3的质量分数为 。
(4)深入研究发现,是述实验方案存在缺陷,致使测得的Na2SO3质量分数偏小,试分析其中的原因(列出一条即可) 。
(Ⅱ)乙同学设计了另一套实验装置如下图:
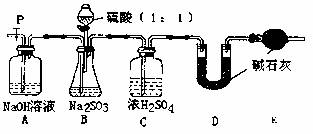
(5)实验中待锥形瓶中不再产生气体后,打开活塞P从导管左端缓缓鼓入一定量的空气,这样做的目的是 。
(6)除已称量的a g Na2SO4样品外,实验中还应测定的数据是 (填图中字母)装置实验前后的质量差。
(Ⅲ)现有以下试剂:蒸馏水、盐酸、稀硝酸、BaC12溶液、Ba(NO3)2溶液。
(7)丙同学欲从中选择合适试剂,来测定已知质量为a g的Na2SO3样品中Na2SO3的质量分数,下述实验方案理论上可行的有 。
A.将样品溶解,加足量盐酸,再加足量BaC12溶液,过滤、洗涤、干燥、称量沉淀m1g
B.将样品溶解,加足量盐酸,再加足量BaC12溶液,过滤、洗涤、干燥、称量沉淀m2g
C.将样品溶解,加过量BaC12溶液,过滤后,将虑液蒸干,称量得固体m3g
D.将样品溶液,加过量Ba(NO3)2溶液,过滤、洗涤,在沉淀中加入足量盐酸,再过滤、洗涤、干燥、称量得固体m4g
查看习题详情和答案>>长期存放的Na2SO3会被空气中的氧气部分氧化:某化学兴趣小组通过实验测定某无水Na2SO3被氧化的程度。
(Ⅰ)甲同学设计了下图实验
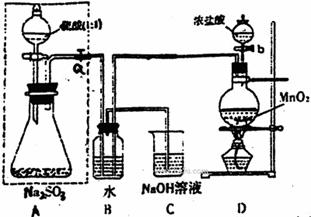
请回答:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应如何检查虚线框内装置的气密性?
。
(2)写出B装置中的离子方程式 。
写出D装置中反应的化学方程式 。
(3)称量agNa2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量BaCl2溶液
充分反应,过滤、洗涤、干燥、称量得白色沉淀bg,则样品中Na2SO3的质量分数为 。
(4)深入研究发现,上述实验方案存在缺陷,致使测得的Na2SO3质量分数偏小,试分析其中的原因(列出一条即可) 。
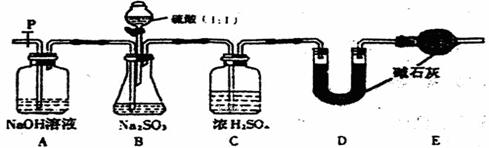 (Ⅱ)乙同学设计了另一套实验装置如下图:
(Ⅱ)乙同学设计了另一套实验装置如下图:
(5)实验中待锥形瓶中不再产生气体后,打开活塞P从导管左端缓缓鼓入一定量的空气,这样做的目的是 。
(6)除已称量的a g Na2SO3样品外,实验中还应测定的数据是 处,(填图中字母)装置实验前后的质量差。
(Ⅲ)现有以下试剂:蒸馏水、盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液。
丙同学欲从中选择合适试剂,来测定已知质量为a g的Na2SO3样品中Na2SO3的质
量分数。下述实验方案理论上可行的有 。
A.将样品溶解,加足量盐酸,再加足量BaCl2溶液,过滤、洗涤、干燥、称量得沉淀ml g
B.将样品溶解,加足量硝酸,再加足量BaCl2溶液、过滤、洗涤、干燥、称量得沉淀m2 g
C.将样品溶解,加过量BaCl2溶液,过滤后将溶液蒸干,称量得固体m3g
D.将样品溶解,加过量Ba(NO3)2溶液,过滤、洗涤,在沉淀中加入足量盐酸,再过滤,洗涤、干燥,称量得固体m4g。
查看习题详情和答案>>(14分)长期存放的Na2SO3,会被空气中的氧气部分氧化。某化学兴趣小组通过实验测定某无水Na2SO3,被氧化的程度。
(Ⅰ)甲同学设计了下图实验。

请回答:
(1)写出B装置中反应的离子方程式 ;
(2)写出D装置中反应的化学方程式 ;
(3)若起始实验时称量出放入锥形瓶中Na2SO3样品质量为a g,实验后向B装置的溶液中加入足量BaCl2溶液充分反应,过滤、洗涤、干燥、称量得白色沉淀b g,则样品中Na2SO3的质量分数为 ;
(4)深入研究发现,上述实验方案存在缺陷,致使测得的Na2SO3,质量分数偏小,试分析其中的原因(列出一条即可) 。
(Ⅱ)乙同学设计了另一套实验装置如下图:

(5)实验中待锥形瓶中不再产生气体后,打开活塞P从导管左端缓缓鼓入一定量的空气,这样做的目的是 ;
(6)除已称量的a g Na2SO3,样品外,实验中还应测定的数据是 处(填图中字母)装置实验前后的质量差。
(Ⅲ)现有以下试剂:蒸馏水、盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液。
(7)丙同学欲从中选择合适试剂,来测定已知质量为ag的Na2SO3,样品中Na2SO3的质量分数,下述实验方案理论上可行的有 。
A. 将样品溶解,加足量盐酸,再加足量BaCl2溶液,过滤、洗涤、干燥、称量得沉淀m
B.将样品溶解,加足量硝酸,再加足量BaCl2溶液,过滤、洗涤、干燥、称量得沉淀m2 g
C.将样品溶解,加过量BaCl2溶液,过滤后,将滤液蒸干,称量得固体m3 g
D.将样品溶解,加过量Ba(NO3)2溶液,过滤、洗涤,在沉淀中加入足量盐酸,再过滤、洗涤、于燥、称量得固体m4 g
查看习题详情和答案>>
(1)将仪器连接好以后,必须进行的第一步操作是
(2)此实验还必须用到的最重要的仪器是
(3)实验室中备有以下常用试剂:
a.浓硫酸 b.品红溶液 c.酸性高锰酸钾溶液 d.饱和碳酸氢钠溶液 e.氢氧化钠溶液
f.无水硫酸铜 g.碱石灰 h.五氧化二磷 i.无水氯化钙
请将下列容器中应盛放的试剂序号填入相应空格:B中
(4)实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的空气.这样做的目的是
所通空气应先经过
(5)若要提高实验的准确性,还应在