网址:http://m.1010jiajiao.com/timu_id_1726614[举报]
已知乙二酸( HOOC—COOH)俗称草酸,它是一种易溶于水的二元弱酸,酸性强于碳酸,其盐草酸钙和草酸氢钙均为白色不溶物。无色晶体H2C2O4·2H2O称为草酸晶体,其熔点为101.5℃。草酸晶体失去结晶水得无水草酸,它在157℃升华。
根据上述信息,回答下列问题。
(1)向盛有2mL饱和NaHCO3溶液的试管里加入约2mL乙二酸浓溶液,观察到的现象是 ,写出该反应的离子方程式: 。
(2)配平乙二酸与酸性KMnO4溶液反应的离子方程式:
MnO4- + H2C2O4 + H+ — Mn2+ + CO2↑+ H2O
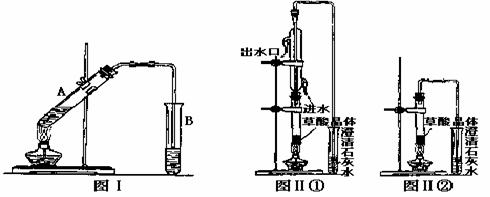
(3)向试管A中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙二酸溶液,按下图Ⅰ连接好装置,加热3—5min。在装有饱和Na2CO3溶液的试管B中有油状且带有香味的液体产生。B中导管口在液面上而不伸入液面下的原因是 。写出乙二酸与足量乙醇完全酯化的化学反应方程式 。
(4)已知草酸分解的化学方程式为:![]() 。
。
利用图Ⅱ①和图Ⅱ②加热草酸晶体,以验证草酸受热是否分解。连续加热一段时间后的现象是:图Ⅱ①:试管里澄清石灰水先变浑浊,后又变澄清,其原因是 ;图Ⅱ②:试管里澄清石灰水只变浑浊,其原因是 ;能验证草酸受热分解的装置是 (填图Ⅱ中的编号“①”或“②”),理由是: (从装置的特点分析)。
查看习题详情和答案>>