网址:http://m.1010jiajiao.com/timu_id_1725890[举报]
 (2011?武汉模拟)某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(2011?武汉模拟)某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:(一)制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是
(2)步骤③中洗涤沉淀的操作是
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较,用右图装置进行实验,实验时均以生成25mL气体为准,其它可能影响实验的因素均已忽略,相关数据见表:
| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤ | 1.2g | CuO 0.5g | |
| ⑥ | 1.2g | MnO2 0.5g |
(3)上述实验中的“待测数据”指
(4)本实验装置图中量气装置B由干燥管、乳胶管和50mL滴定管改造后组装而成,此处所用滴定管是
(5)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
(6)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a.

(1)盐酸与菱锰矿中碳酸锰反应的化学方程式为
(2)酸浸取时,浸出时间对浸出率的影响如图2所示,工业采用的浸取时间是60min,其可能的原因是
(3)图1中“净化剂X”可能是
(4)加入MnSO4后控制实验条件析出某种杂质离子的盐Y,盐Y的主要成分是
(5)浓缩结晶时,必须一出现晶膜就立刻停止加热,其原因是
(15分)广义的化学反应速率可以用参加化学反应的任一种物质“在单位时间内某一可测的物理量的变化量”来表示,即V(A) = ![]() ,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
可选用试剂及规格:纯锌、粗锌(含铜杂质)、1mol/L 稀硫酸、2mol/L 稀硫酸,
反应温度:250C、350C
(1)请写出锌和硫酸反应的离子方程式
(2)为表达锌和硫酸反应快慢,该学习小组设计了如下表格,请填充表格丁、戊、己三处。
| 编号 | 反应速率表达式的定义 | 反应速率表达式 | 反应速率单位 |
| ① | 单位时间内H+浓度的变化量 | V(H+) = | mol / L.min |
| ② | 丁 | 戊 | 己 |
| ③ | 单位时间内生成H2标况下的体积 | V(H2) = | L / min |
(3)该学习小组选用0.1 mol Zn和200 mL 1mol/L 稀硫酸(硫酸过量)在250C反应进行研究,用秒表计时,至锌块完全溶解且溶液中不再有气泡放出时,记录反应时间为5分钟,该反应速率V(H+) =
(4)该小组对“影响反应速率的因素”进行了分析,设计如下系列实验,庚辛壬癸四处空白。
| 编号 | 锌的形状 | 锌的规格 | 硫酸的浓度 | 反应温度 | 实验设计的目的 |
| ① | 块状 | 纯锌 | 1mol/L | 250C | 实验①和②研究的目的是 庚 ;
实验②和③研究硫酸浓度对反应速率影响; 实验③和④研究锌的规格对反应速率影响;
实验④和⑤研究的目的是 癸 ;
|
| ② | 颗粒状 | 纯锌 | 1mol/L | 250C | |
| ③ | 颗粒状 | 纯锌 | 辛 | 250C | |
| ④ | 颗粒状 | 壬 | 2mol/L | 250C | |
| ⑤ | 颗粒状 | 粗锌 | 2mol/L | 350C | |
| …… |
查看习题详情和答案>>
(15分)广义的化学反应速率可以用参加化学反应的任一种物质“在单位时间内某一可测的物理量的变化量”来表示,即V(A) =  ,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。

可选用试剂及规格:纯锌、粗锌(含铜杂质)、1mol/L 稀硫酸、2mol/L 稀硫酸,
反应温度:250C 、350C
(1)请写出锌和硫酸反应的离子方程式
(2)为表达锌和硫酸反应快慢,该学习小组设计了如下表格,请填充表格丁、戊、己三处。
|
编号 |
反应速率表达式的定义 |
反应速率表达式 |
反应速率单位 |
|
① |
单位时间内H+浓度的变化量 |
V(H+) = |
mol / L.min |
|
② |
丁 |
戊 |
己 |
|
③ |
单位时间内生成H2标况下的体积 |
V(H2) = |
L / min |
(3)该学习小组选用0.1 mol Zn和200 mL 1mol/L 稀硫酸(硫酸过量)在250C反应进行研究,用秒表计时,至锌块完全溶解且溶液中不再有气泡放出时,记录反应时间为5分钟,该反应速率V(H+) =
(4)该小组对“影响反应速率的因素”进行了分析,设计如下系列实验,庚辛壬癸四处空白。
|
编号 |
锌的形状 |
锌的规格 |
硫酸的浓度 |
反应温度 |
实验设计的目的 |
|
① |
块状 |
纯锌 |
1mol/L |
250C |
实验①和②研究的目的是 庚 ;
实验②和③研究硫酸浓度对反应速率影响; 实验③和④研究锌的规格对反应速率影响;
实验④和⑤研究的目的是 癸 ;
|
|
② |
颗粒状 |
纯锌 |
1mol/L |
250C |
|
|
③ |
颗粒状 |
纯锌 |
辛 |
250C |
|
|
④ |
颗粒状 |
壬 |
2mol/L |
250C |
|
|
⑤ |
颗粒状 |
粗锌 |
2mol/L |
350C |
|
|
…… |
查看习题详情和答案>>
将1molCO和1molH2O充入某固定容积的反应器中,在某条件下达到平衡:
CO+H2O(g)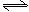 CO2+H2,此时有2/3的CO转化为CO2。
CO2+H2,此时有2/3的CO转化为CO2。
(1)该平衡混合物中CO2的体积分数为
(2)若容器体积为1L,到达平衡所需时间为2分钟,则H2的平均反应速率为
(3)若在相同条件下,向容器中充入1molCO2、1molH2和1molH2O,则达到平衡时与⑴中平衡相比较,平衡应向 (填“正反应方向”、“逆反应方向”或“不”)移动,此时平衡混合物中CO2的体积分数可能是下列各值中的
| A.22.2% | B.27.55% | C.33.3% | D.36.8% |
①生成物的产量一定增加; ②生成物的体积分数一定增加;
③反应物的转化率一定增大; ④反应物的浓度一定降低;
⑤正反应速率一定大于逆反应速率; ⑥一定使用了催化剂. 查看习题详情和答案>>

