摘要:11.X.Y.Z是三种短周期元素.X.Y位于同一主族.Y.Z处于同一周期.X元素原子的最外层电子数是其电子层数的3倍.Z元素原子的核外电子数比Y原子少1.下列说法正确的是 A.元素原子得电子能力强弱顺序为Z>Y>X B.Y元素最高价氧化物对应的水化物的化学式为 C.三种元素的气态氢化物中.Z的气态氢化物最稳定 D.原子半径大小顺序为Z>Y>X
网址:http://m.1010jiajiao.com/timu_id_1725355[举报]
短周期元素X、Y、Z在元素周期表中的位置如右图,关于X、Y、 Z的说法正确的是( )
| A.相同条件下,三种元素的单质跟氢气反应时,X单质最剧烈 |
| B.Y的气态氢化物稳定性比Z的气态氢化物的稳定性强 |
| C.ZO2能与Z的最高价氧化物对应的水化物反应生成Z单质 |
| D.由氢、氧和Z元素形成的常见化合物中既含有离子键又含有共价键 |
短周期元素X、Y、Z在元素周期表中的位置如右图,关于X、Y、 Z的说法正确的是( )
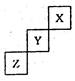
A.相同条件下,三种元素的单质跟氢气反应时,X单质最剧烈
B.Y的气态氢化物稳定性比Z的气态氢化物的稳定性强
C.ZO2能与Z的最高价氧化物对应的水化物反应生成Z单质
D.由氢、氧和Z元素形成的常见化合物中既含有离子键又含有共价键
查看习题详情和答案>>
短周期元素X、Y、Z在元素周期表中的位置如图,关于X、Y、 Z的说法正确的是 ( )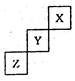
| A.相同条件下,三种元素的单质跟氢气反应时,X单质最剧烈 |
| B.由氢、氧和Z元素形成的常见化合物中既含有离子键又含有共价键 |
| C.ZO2能与Z的最高价氧化物对应的水化物反应生成Z单质 |
| D.Y的气态氢化物稳定性比Z的气态氢化物的稳定性强 |
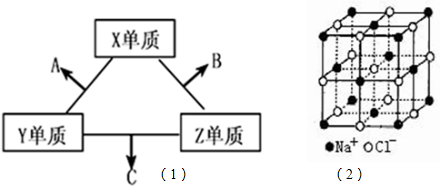
短周期元素在元素中占有重要地位.X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如(1)变化:
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是______周期______族.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在______.
(3)在C分子中,Y原子的杂化方式为______,与Y原子同主族在第四周期的元素原子基态电子排布式是______.
(4)NaCl的晶体结构如图(2)所示,若将晶胞面心和体心的原子除去,顶点的钠离子换为Xn+(X代表某元素符号)离子,棱上的Cl-换为O2-,就得到X的氧化物的晶体结构.则该X的氧化物的化学式为______.
查看习题详情和答案>>
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是______周期______族.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在______.
(3)在C分子中,Y原子的杂化方式为______,与Y原子同主族在第四周期的元素原子基态电子排布式是______.
(4)NaCl的晶体结构如图(2)所示,若将晶胞面心和体心的原子除去,顶点的钠离子换为Xn+(X代表某元素符号)离子,棱上的Cl-换为O2-,就得到X的氧化物的晶体结构.则该X的氧化物的化学式为______.

四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题.
(1)Z在元素周期表中位于______族.
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其它三种物质发生化学反应,该元素是______(填元素符号).
(3)①下列可作为比较X和Y金属性强弱的依据是______ (填序号).
a.自然界中的含量 b.相应氯化物水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②从原子结构的角度解释X的金属性强于Y的原因:______,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y.
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是______,混合后溶液中离子浓度由大到小的顺序是______.
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数.

能确定混合物中Y的质量分数的数据有______(填序号).
a.m、n b.m、y c.n、y.
查看习题详情和答案>>
| W | X | Y | Z | |
| 结构 或性质 |
最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最低负价之和为零 |
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其它三种物质发生化学反应,该元素是______(填元素符号).
(3)①下列可作为比较X和Y金属性强弱的依据是______ (填序号).
a.自然界中的含量 b.相应氯化物水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②从原子结构的角度解释X的金属性强于Y的原因:______,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y.
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是______,混合后溶液中离子浓度由大到小的顺序是______.
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数.

能确定混合物中Y的质量分数的数据有______(填序号).
a.m、n b.m、y c.n、y.