摘要:19. 用脱脂药棉包住约0.2g过氧化钠粉末.置于石棉网上.往脱脂棉上滴水.可观察到脱脂棉剧烈燃烧起来. (1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:第一.有氧气生成,第二. .过氧化钠跟水反应的化学方程式为 . (2)某研究性学习小组拟用下图所示装置进行实验.以证明(1)的结论. 用以验证第一条结论的实验方法是 .为了验证第二条结论.将管口b浸入水中.可观察到的现象为为了验证第二条结论.将管口b浸入水中.可观察到的现象为 .
网址:http://m.1010jiajiao.com/timu_id_1725190[举报]
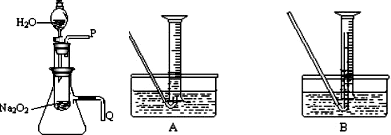 (2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
第一:有氧气生成;第二:
该反应是放热反应
该反应是放热反应
.Na2O2跟水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(2)某研究性学习小组拟用右图所示装置(气密性良好)
进行实验,以证明上述结论.
用以验证第一条结论的实验操作是:
打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O2生成
打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O2生成
;用以验证第二条结论的实验方法是:
将导管Q浸入水中,反应过程中导管口有气泡冒出
将导管Q浸入水中,反应过程中导管口有气泡冒出
.(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色.为探究其原因,该小组同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性.请设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在.(只要求写出实验所用的试剂及观察到的现象)
试剂:
MnO2
MnO2
;现象:气泡迅速产生,能使带火星的木条复燃
气泡迅速产生,能使带火星的木条复燃
.(4)该小组同学提出用定量的方法探究Na2O2跟水反应后的溶液中否含有H2O2,其实验方法为:称取2.6g Na2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论.
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积)
B
B
(填序号),理由是防止气体冷却时发生倒吸现象
防止气体冷却时发生倒吸现象
.②若在标准状况下测量气体的体积,应选用的量筒的大小规格为
500mL
500mL
(选填“100mL”“200mL”“500mL”或“1000mL”).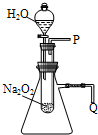 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.(1)由上述实验现象所得到的过氧化钠跟水反应的结论是:
①有氧气生成;②反应过程中有
(2)Na2O2跟水反应的化学方程式为
(3)某研究性学习小组拟用右图所示装置(气密性良好)进行实验,以证明上述实验结论.验证第①条结论的实验操作及现象是:向试管中滴入水,
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,现象为
 (1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na2O2和H2O反应的结论是:
(1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na2O2和H2O反应的结论是:ab
ab
a:有氧气生成 b:反应放热.
(2)Na2O2和H2O反应的化学方程式是
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(3)某研究性学习小组拟用如图的装置进行实验,以证明上述结论.用以验证结论a的实验方法是:
打开活塞(或阀门)向试管内包有过氧化钠的石棉网上滴几滴水,用带火星的木条靠近p,木条复燃
打开活塞(或阀门)向试管内包有过氧化钠的石棉网上滴几滴水,用带火星的木条靠近p,木条复燃
(4)用以验证结论b的实验方法及现象是:
把q插入盛水的小烧杯中,有气泡冒出.
把q插入盛水的小烧杯中,有气泡冒出.
.