摘要:HCO3-+H2OH2CO3+OH-.HCO3-的水解程度大于电离程度 △(2)NH4++OH- ===NH3↑+H2O 2NH3+4H3BO3=2NH4++B4O72―+5H2O
网址:http://m.1010jiajiao.com/timu_id_172518[举报]
人体血液的正常pH约为7.35~7.45,若在外界因素作用下突然发生改变就会引起“酸中毒”或“碱中毒”,甚至有生命危险。由于人体体液的缓冲系统中存在如下平衡:
H++HCO3- H2CO3
H2CO3 CO2+H2O
CO2+H2O
H++PO43- HPO42-
HPO42-
H++HPO42- H2PO4-
H2PO4-
故能维持血液pH的相对稳定,以保证正常生理活动。下列说法中不合理的是
| A.当强酸性物质进入人体的体液后,上述缓冲系统的平衡向右移,从而维持pH稳定 |
| B.当强碱性物质进入人体的体液后,上述缓冲系统的平衡向左移,从而维持pH稳定 |
| C.某病人在静脉滴注的大量生理盐水后,血液被稀释,会导致c(H+)显著减少,pH值显著增大,可能会引起碱中毒 |
| D.在人体进行呼吸活动时,如CO2进入血液,会使平衡向左移动,c(H+)增大,pH值略减小 |
关于小苏打水溶液的表述正确的是
[ ]
A.c(Na+) =c(HCO3-)+c(CO32-)+c(H2CO3)
B. c(Na+)+c( H+) =c(HCO3-)+c(CO32-)+c(OH-)
C.HCO3-的电离程度大于HCO3-的水解程度
D.存在的电离有:NaHCO3==Na++HCO3-,HCO3- H++CO32- ,H2O
H++CO32- ,H2O H++OH-
H++OH-
查看习题详情和答案>>
B. c(Na+)+c( H+) =c(HCO3-)+c(CO32-)+c(OH-)
C.HCO3-的电离程度大于HCO3-的水解程度
D.存在的电离有:NaHCO3==Na++HCO3-,HCO3-
 H++CO32- ,H2O
H++CO32- ,H2O H++OH-
H++OH- 关于小苏打水溶液的表述正确的是
[ ]
A.c(Na+)=c(HCO3-)+2c(CO32-)+c(H2CO3)
B.c(Na+)+c(H+) =c(HCO3-)+c(CO32-)+c(OH-)
C.HCO3-的电离程度大于HCO3-的水解程度
D.存在的电离有:NaHCO3=Na++HCO3- HCO3- H++CO32- H2O
H++CO32- H2O H++OH-
H++OH-
查看习题详情和答案>>
B.c(Na+)+c(H+) =c(HCO3-)+c(CO32-)+c(OH-)
C.HCO3-的电离程度大于HCO3-的水解程度
D.存在的电离有:NaHCO3=Na++HCO3- HCO3-
 H++CO32- H2O
H++CO32- H2O H++OH-
H++OH- 某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:

(1)补全上述①②③④各步反应的离子方程式
①Mg+2H+═Mg2++H2↑,
②
③
④2A1(OH)3═Al203+H20
(2)该样品中铝的质量分数是
×100%
×100%
(3)第②步中加入Na0H溶液不足时,会使测定结果
第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果
A.偏高 B.偏低 C.不影响.
查看习题详情和答案>>

(1)补全上述①②③④各步反应的离子方程式
①Mg+2H+═Mg2++H2↑,
2Al+6H+═2Al3++3H2↑
2Al+6H+═2Al3++3H2↑
②
H++OH-=H2O
H++OH-=H2O
,Al3++4OH-═AlO2-+2H2O
Al3++4OH-═AlO2-+2H2O
Mg2++OH-═Mg(OH)2↓ ③
OH-+CO2=HCO3-
OH-+CO2=HCO3-
CO2+H20+A102-═Al(OH)3↓+HCO3- ④2A1(OH)3═Al203+H20
(2)该样品中铝的质量分数是
| 54b |
| 102a |
| 54b |
| 102a |
(3)第②步中加入Na0H溶液不足时,会使测定结果
B
B
第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果
A
A
第④步对沉淀灼烧不充分时,会使测定结果A
A
A.偏高 B.偏低 C.不影响.
 (2009?广东)超细氧化铝是一种重要的功能陶瓷原料.
(2009?广东)超细氧化铝是一种重要的功能陶瓷原料.(1)实验室常以NH4Al(SO4)2和NH4HCO3为原料,在一定条件下先反应生成沉淀NH4AlO(OH)HCO3该沉淀高温分解即得超细Al2O3.NH4AlO(OH)HCO3热分解的化学反应方程式
2NH4AlO(OH)HCO3 Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑
 Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑2NH4AlO(OH)HCO3 Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑
. Al2O3+3H2O↑+2CO2↑+2NH3↑
Al2O3+3H2O↑+2CO2↑+2NH3↑(2)NH4Al(SO4)2?12H2O的相对分子质量为453.欲配制100mLPH为2、浓度约为0.1mol-1的NH4Al(SO4)2溶液,配制过程为
①用托盘天平称量NH4Al(SO4)2?12H2O固体
4.5
4.5
g;②将上述固体置于烧杯中
用量筒量取100mL水,搅拌溶解,用H2SO4调节溶液PH至2
用量筒量取100mL水,搅拌溶解,用H2SO4调节溶液PH至2
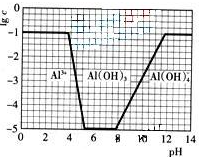
.(3)在0.1mol?L-1NH4Al(SO4)2溶液中,铝各形态的浓度(以Al3+计)的对数(lgc)随溶液PH变化的关系见下图
①用NaOH溶液调节(2)中溶液PH至7,该过程中发生反应的离子方程式有
H++OH-=H2O、Al3++3OH-=Al(OH)3↓、NH4++OH-=NH3?H2O
H++OH-=H2O、Al3++3OH-=Al(OH)3↓、NH4++OH-=NH3?H2O
.②请在答题卡的框图中,画出0.01mol?L-1NH4Al(SO4)2溶液中铝各形态的浓度的对数lgc随溶液PH变化的关系图,并进行必要的标注.