网址:http://m.1010jiajiao.com/timu_id_1724759[举报]
(13分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B—少一个电子层,B原子得一个电子填入3p轨道后, 3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2—离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体属于密置堆积方式,则其晶体晶胞类型属于 。(填写“六方”、“面心立方”或“体心立方”)。
(2)B—的电子排布式 ,在CB3分子中C元素原子的原子轨道发生的是_______杂化。
(3)C的氢化物空间构型为 ,其氢化物在同族元素所形成的氢化物中沸点最高的原因是 。
(4)B元素的电负性 D元素的电负性(填“>”,“<”或“=”);用一个化学方程
式说明B、D两元素形成的单质的氧化性强弱: 。
(5)如上图所示是R形成的晶体的晶胞,设晶胞的边
长为acm。则R晶体的密度为 。(阿伏加德数常数用NA表示)
查看习题详情和答案>>
(14分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度是同族元素所形成的氢化物中最大的;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2∶1。请回答下列问题:
⑴A单质、B单质、化合物R的熔点大小顺序为下列的 (填序号):
①A单质>B单质>R; ②R>A单质>B单质;
③B单质>R >A单质; ④A单质>R>B单质。
⑵在CB3分子中C元素原子的原子轨道发生的是________杂化,其固体的晶体类型为 ;
⑶写出D原子的核外价电子排布式 _,C的氢化物比D的氢化物在水中溶解度大得多的可能原因
;
⑷右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体
中阴、阳离子数之比为 ,FeD2物质中具有的化
学键类型为 。
查看习题详情和答案>>
(13分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B—少一个电子层,B原子得一个电子填入3p轨道后, 3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2—离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体属于密置堆积方式,则其晶体晶胞类型属于 。(填写“六方”、“面心立方”或“体心立方”)。
(2)B—的电子排布式 ,在CB3分子中C元素原子的原子轨道发生的是_______杂化。
(3)C的氢化物空间构型为 ,其氢化物在同族元素所形成的氢化物中沸点最高的原因是 。
(4)B元素的电负性 D元素的电负性(填“>”,“<”或“=”);用一个化学方程
式说明B、D两元素形成的单质的氧化性强弱: 。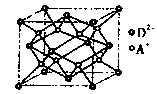
(5)如上图所示是R形成的晶体的晶胞,设晶胞的边
长为acm。则R晶体的密度为 。(阿伏加德数常数用NA表示)
(14分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度是同族元素所形成的氢化物中最大的;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2∶1。请回答下列问题:
⑴A单质、B单质、化合物R的熔点大小顺序为下列的 (填序号):
①A单质>B单质>R; ②R>A单质>B单质;
③B单质>R >A单质; ④A单质>R>B单质。
⑵在CB3分子中C元素原子的原子轨道发生的是________杂化,其固体的晶体类型为 ;
⑶写出D原子的核外价电子排布式 _,C的氢化物比D的氢化物在水中溶解度大得多的可能原因
;
⑷右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体
中阴、阳离子数之比为 ,FeD2物质中具有的化
学键类型为 。
(13分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B—少一个电子层,B原子得一个电子填入3p轨道后, 3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2—离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体属于密置堆积方式,则其晶体晶胞类型属于 。(填写“六方”、“面心立方”或“体心立方”)。
(2)B—的电子排布式 ,在CB3分子中C元素原子的原子轨道发生的是_______杂化。
(3)C的氢化物空间构型为 ,其氢化物在同族元素所形成的氢化物中沸点最高的原因是 。
(4)B元素的电负性 D元素的电负性(填“>”,“<”或“=”);用一个化学方程
式说明B、D两元素形成的单质的氧化性强弱: 。
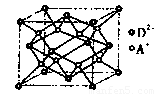
(5)如上图所示是R形成的晶体的晶胞,设晶胞的边
长为acm。则R晶体的密度为 。(阿伏加德数常数用NA表示)
查看习题详情和答案>>