摘要:16.经X射线分析鉴定.钛酸钡晶体属于立方晶系(如下图所示.且.和互相接触)下列说法不正确的是 A.该晶体化学式为 B.该晶体属于离子晶体.熔点较高 C.与配位的氧离子构成正四面体 D.与配位的氧离子个数为12 第Ⅱ卷
网址:http://m.1010jiajiao.com/timu_id_1724753[举报]
(8分)经X射线分析鉴定,某一离子晶体属于立方晶系,其晶胞参数a = 403.1 pm。晶胞顶点位置为Ti4+ 所占,体心位置为Ba2+ 所占,所有棱心位置为O2-所占。请据下图回答或计算:
(1) 用分数坐标表达诸离子在晶胞中的位置:
(2) 写出此晶体的化学组成:
(3) 指出晶体的点阵型式、结构基元:
(4) 指出Ti4+ 的氧配位数与Ba2+ 的氧配位数及O2-的配位情况:
(5) 计算两种正离子半径值:
(6) Ba2+ 和O2-联合组成哪种型式堆积:
查看习题详情和答案>>(三选一)【选修三:物质结构与性质]
热敏电阻PTC元件的主要成份为钡钛矿,其晶体结构如图所示,该结构是具有代表性的最小重复单位。该晶体经X射线分析鉴定:重复单位为正方体,边长为403.1pm,顶点位置为Ti4+所占,体心位置为Ba2+所占,所有核心位置为O2-所占。
回答下列问题:
热敏电阻PTC元件的主要成份为钡钛矿,其晶体结构如图所示,该结构是具有代表性的最小重复单位。该晶体经X射线分析鉴定:重复单位为正方体,边长为403.1pm,顶点位置为Ti4+所占,体心位置为Ba2+所占,所有核心位置为O2-所占。
回答下列问题:
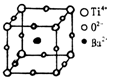
(1)钛的原子序数为22,其次外层有2个单电子,写出钛原子基态时核外电子排布式:___________________。
(2)写出晶体的化学式:_________________。
(3)若Ti4+位于晶胞的体心,Ba2+位于晶胞的顶点,则O2-处于立方体的位置是____________________________。
(4)在该物质晶体中,每个Ti4+周围与它最邻近且距离相等的Ti4+有__________个,它们在空间构成的形状是:______________。
(5)已知O2-半径为140pm,则Ti4+的半径为___________。
查看习题详情和答案>>
(2)写出晶体的化学式:_________________。
(3)若Ti4+位于晶胞的体心,Ba2+位于晶胞的顶点,则O2-处于立方体的位置是____________________________。
(4)在该物质晶体中,每个Ti4+周围与它最邻近且距离相等的Ti4+有__________个,它们在空间构成的形状是:______________。
(5)已知O2-半径为140pm,则Ti4+的半径为___________。
(9分)Ar、Xe、CH4、Cl2等分子能和水形成气体水合物晶体。在这种晶体中,水分子形成三维氢键骨架体系。在骨架中有空穴,它可以容纳这些气体小分子形成笼型结构。
4-1 甲烷的气体水合物晶体成为可燃冰。已知每1m3这种晶体能释放出164m3的甲烷气体。试估算晶体中水与甲烷的分子比。(不足的数据由自己假定,只要假设合理均按正确论)
4-2 X-射线衍射分析表明,该晶体属于立方晶系a=1200pm。晶胞中46个水分子围成两个五角十二面体和六个稍大的十四面体(2个六角形面,12个五角形面),八个CH4分子可以进入这些多面体笼中。计算甲烷和水的分子数之比和该晶体的密度。
4-3 已知Cl2的气体水合物晶体中,Cl2和H2O的分子数之体为18,在其晶体中水分子所围成的笼型结构与可燃冰相同。推测它的结构。
查看习题详情和答案>>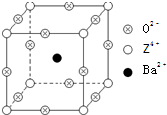 (2011?江西二模)已知X、Y和Z三种元素的原子序数之和等于48.X的一种1:1型氢化物分子中既有σ键又有π键.Z是金属元素,Z的单质和化合物有广泛的用途.已知Z的核电荷数小于28,且次外层有2个未成对电子.工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐).M有显著的“压电性能”,应用于超声波的发生装置.经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.
(2011?江西二模)已知X、Y和Z三种元素的原子序数之和等于48.X的一种1:1型氢化物分子中既有σ键又有π键.Z是金属元素,Z的单质和化合物有广泛的用途.已知Z的核电荷数小于28,且次外层有2个未成对电子.工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐).M有显著的“压电性能”,应用于超声波的发生装置.经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.(1)Y在周期表中位于
第四周期第ⅡA族
第四周期第ⅡA族
;Z4+的核外电子排布式为1s22s22p63s23p6
1s22s22p63s23p6
;(2)X的该种氢化物分子构型为
直线型
直线型
,X在该氢化物中以sp
sp
方式杂化.X和Y形成的化合物的熔点应该高于
高于
(填“高于”或“低于”)X氢化物的熔点.(3)①制备M的化学反应方程式是
TiO2+BaCO3═BaTiO3+CO2↑
TiO2+BaCO3═BaTiO3+CO2↑
;②在M晶体中,若将Z4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-处于立方体的
面心
面心
;③在M晶体中,Z4+的氧配位数为
6
6
;④已知O2-半径为1.40×10-10 m,则Z4+半径为
6.15×10-11
6.15×10-11
m.