网址:http://m.1010jiajiao.com/timu_id_1724469[举报]
| A、含18个电子的气态分子M在水中分步电离出两种阴离子,则其钠盐显碱性,只能与酸反应 | B、X、Y均为短周期元素,其简单离子mXa+与nYb-的电子层结构相同,则m>n,离子半径:mXa+>nYb- | C、结合质子(H+)能力:OH->CO32->CH3COO->NO3- | D、若两种微粒的质子数和电子数都相同,则这两种微粒可能是一种分子和一种阳离子 |
下列叙述正确的是( )
A. 若X的质子数为a,中子数为b,则X的质量数为:a-b
B. 若![]() ,则氧化性:
,则氧化性:![]()
C. 若![]() 和M+的电子层结构相同,则原子序数:R>M
和M+的电子层结构相同,则原子序数:R>M
D. 若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:![]()
X、Y、Z、R 四种短周期元素,原子序数依次增大。已知:X、R处于同一主族,Y元素的最高正价和最低负价的绝对值相等,X与Y元素形成的一种物质是天然气的主要成分;Y与Z元素形成的一种气体会使大气产生“温室效应”。
请回答下列问题:
(1)X、Y、Z三元素所形成的单质或化合物之间,可按下图装置组成燃料电池。
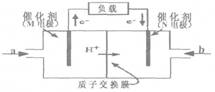
若b口通入的是气体Z2,则a口通入的物质可以是 、 、 (分别填写只由一种、两种、三种元素组成的物质,用化学式表示);M电极的名称为 (填“正极”、“负极”或“阴极”、“阳极”);N电极的电极反应式为 (用化学式表示)。
(2)日常生活中我们经常用到的一种物质其主要成分的化学式为Y18X35Z2R,这种物质的学名为 ,制造这种物质的反应叫 ,写出该反应的化学方程式 。
(3)合成氨工业中,原料气制备的其中一个反应为:YZ+X2Z(g)![]() YZ2+X2;
YZ2+X2;
已知该反应化学平衡常数K和温度T的关系如下表:
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
则下列有关的叙述正确的是 。
A.该反应![]() <0
<0
B.若绝热时(容器内外没有热量交换),改变某一条件平衡向逆反应方向移动,刚容器内气体的温度一定升高
C.若反应在830℃的温度达到平衡状态,反应容器内的四种物质的浓度则一定相等
D.该反应在某温度下,YZ、X2Z的物质的量浓度与时间的关系如下图所示,据此可计算得YZ的转化率为80%

A、B、C、D是短周期元素形成的四种气体单质,其它物质为化合物。H常作为普通锌锰干电池的电解质。有关的转化关系如下图所示(反应条件均已略去)。
请回答下列问题:
(1)B的结构式为____ ,G的化学式为 。
(2)Y和E在一定条件下可反应生成B和Z,该反应的化学方程式为 。
(3)在体积为0.5L的恒容密闭容器中,充人1.25molB和1.25molD进行如下化学反应:
B(g)+3D(g)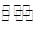 2Y(g),其化学平衡常数K与T的关系如下表所示:
2Y(g),其化学平衡常数K与T的关系如下表所示:
|
T/℃ |
300 |
400 |
|
K |
3.41 |
0.50 |
①若反应在400℃下进行,下列各项中能作为判断该反应达到化学平衡状态依据的是
(填字母)。
A.Y、B、D的物质的量分别为0.50mol、l.0mol、0.50mol
B.v正(B)= 3v 逆(D)
C.容器内压强保持不变
D.混合气体的密度保持不变
②在一定条件下B(g)+3D(g)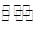 2Y(g)达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是( )
2Y(g)达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是( )
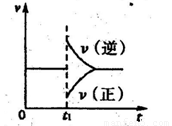
A.维持温度、反应体系体积不变,t1时充入Y(g)
B.维持压强不变,tl时升高反应体系温度
C.维持温度不变,t1时扩大反应体系体积
D.维持温度、压强不变,t1时充入Y(g)
(4)0.lmol·L-1的X溶液和0.2mol·L-1的Y溶液等体积混合后显碱性,则该混合溶液中各离子浓度大小顺序是 .
(5)常温下,0.1mol·L-1的Y溶液中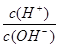 =l×10-8,下列叙述中错误的是 ( )
=l×10-8,下列叙述中错误的是 ( )
A.该溶液的pH=11
B.该溶液中的溶质电离出的阳离子浓度为0.1mol·L-1
C.该溶液中水电离出的c(H+)与c(OH—)乘积为l×10-22
D.pH=l的X溶液V1L与0.1mol·L-1的Y溶液V2L混合,若混合溶液pH =7,则V1<V2
E.将0.1mol·L-1的Y溶液加水稀释100倍后,pH >9
查看习题详情和答案>>
A、B、C、D是短周期元素形成的四种气体单质,其它物质为化合物。H常作为普通锌锰干电池的电解质。有关的转化关系如下图所示(反应条件均已略去)。
请回答下列问题:
(1)B的结构式为____ ,G的化学式为 。
(2)Y和E在一定条件下可反应生成B和Z,该反应的化学方程式为 。
(3)在体积为0.5L的恒容密闭容器中,充人1.25molB和1.25molD进行如下化学反应:
B(g)+3D(g)2Y(g),其化学平衡常数K与T的关系如下表所示:
| T/℃ | 300 | 400 |
| K | 3.41 | 0.50 |
①若反应在400℃下进行,下列各项中能作为判断该反应达到化学平衡状态依据的是
(填字母)。
A.Y、B、D的物质的量分别为0.50mol、l.0mol、0.50mol
B.v正(B)= 3v 逆(D)
C.容器内压强保持不变
D.混合气体的密度保持不变
②在一定条件下B(g)+3D(g)2Y(g)达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是( )
A.维持温度、反应体系体积不变,t1时充入Y(g)
B.维持压强不变,tl时升高反应体系温度
C.维持温度不变,t1时扩大反应体系体积
D.维持温度、压强不变,t1时充入Y(g)
(4)0.lmol·L-1的X溶液和0.2mol·L-1的Y溶液等体积混合后显碱性,则该混合溶液中各离子浓度大小顺序是 .
(5)常温下,0.1mol·L-1的Y溶液中=l×10-8,下列叙述中错误的是 ( )
A.该溶液的pH=11
B.该溶液中的溶质电离出的阳离子浓度为0.1mol·L-1
C.该溶液中水电离出的c(H+)与c(OH—)乘积为l×10-22
D.pH=l的X溶液V1L与0.1mol·L-1的Y溶液V2L混合,若混合溶液pH =7,则V1<V2
E.将0.1mol·L-1的Y溶液加水稀释100倍后,pH >9
查看习题详情和答案>>