摘要:32.[化学--物质结构与性质] 在元素周期表中.一稀有气体元素原子的最外层电子构型为4s24p6.与其同周期的A.B.C.D四种元素.它们的原子的最外层电子数依次为2.2.1.7.其中A.C两元素原子的次外层电子数为8.B.D两元素原子的次外层电子数为18.E.D两元素处于同族.且在该族元素中.E的气态氢化物的沸点最高. (1)B元素在周期表中的位置 . (2)E的气态的氢化物在同族元素中沸点最同的原因是 . (3)A.C两元素第一电离能 > . (4)B元素能形成多种配全物.元素之间形成配合物的条件是:一方是能够提供孤对电子的原子.另一方是 的原子.
网址:http://m.1010jiajiao.com/timu_id_1724318[举报]
[化学-物质结构与性质]
A、B、C、D、E、F六种元素,A、B、C属于第四周期且单质均为固体.原子处于基态时,A、B原子核外电子均成对,且核电荷数A>B;C与A在周期表属于同一区的元素.如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E、F的原子均有三个能层,E原子的第一电离能至第四电离能(kJ/mol)分别为:
578,1817、2745、11575;E与F能形成原子数目比为1:3,熔点为190℃的化合物Q.请回答:
(1)写出A的基态核外电子排布式
(2)C2+和A2+都能与NH3、H2O等形成配位数为4的配合物.[A(NH3)4]2+和[C(NH3)4]2+都具有对称的空间构型,[C(NH3)4]2+中的两个NH3被两个Cl-取代能得到两种不同结构的产物,而[A(NH3)4]2+中的两个NH3被两个Cl-取代只能得到一种产物,则[C(NH3)4]2+的空间构型为
(3)1mol D的单质分子中存在
(4)实验测得气态无水Q在1.01ⅹ105Pa,t1℃的密度为5.00g/L,气体摩尔体积为53.4L/mol,则此时Q的组成为(写化学式)
查看习题详情和答案>>
A、B、C、D、E、F六种元素,A、B、C属于第四周期且单质均为固体.原子处于基态时,A、B原子核外电子均成对,且核电荷数A>B;C与A在周期表属于同一区的元素.如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E、F的原子均有三个能层,E原子的第一电离能至第四电离能(kJ/mol)分别为:

578,1817、2745、11575;E与F能形成原子数目比为1:3,熔点为190℃的化合物Q.请回答:
(1)写出A的基态核外电子排布式
1s22s22p63s23p63d104s2
1s22s22p63s23p63d104s2
;用最简式表示B、C合金的组成CaCu5
CaCu5
用元素符号表示)(2)C2+和A2+都能与NH3、H2O等形成配位数为4的配合物.[A(NH3)4]2+和[C(NH3)4]2+都具有对称的空间构型,[C(NH3)4]2+中的两个NH3被两个Cl-取代能得到两种不同结构的产物,而[A(NH3)4]2+中的两个NH3被两个Cl-取代只能得到一种产物,则[C(NH3)4]2+的空间构型为
平面正方形
平面正方形
.[A(NH3)4]2+中A的杂化方式为sp3
sp3
.(3)1mol D的单质分子中存在
NA
NA
个σ键NA个
NA个
π键.D的气态氢化物很容易与H+结合,C原子与H+间形成的键叫配位键
配位键
.(4)实验测得气态无水Q在1.01ⅹ105Pa,t1℃的密度为5.00g/L,气体摩尔体积为53.4L/mol,则此时Q的组成为(写化学式)
Al2Cl6
Al2Cl6
,Q属于分子
分子
晶体.[化学-物质结构与性质]
W、X、Y、Z 4种元素原子序数依次减小.W的原子序数为24;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能(I)如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
(1)W基态原子的电子排步式为
(2)电负性:X
(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高,原因是:
(4)氨为常见化工原料,氨分子中N原子采用
已知W3+能与氨分子形成配离子[W(NH3)6]3+,该配离子中存在的化学键有
A.金属键 B.离子键 C.共价键 D.配位键.
查看习题详情和答案>>
W、X、Y、Z 4种元素原子序数依次减小.W的原子序数为24;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能(I)如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 | I5 |
| Y | 584 | 1823 | 2751 | 11584 | 14837 |
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
.(2)电负性:X
>
>
Y(填“>”、“=”或“<”).(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高,原因是:
氟化氢分子间形成了氢键,而氯化氢分子间只有范德华力.
氟化氢分子间形成了氢键,而氯化氢分子间只有范德华力.
.(4)氨为常见化工原料,氨分子中N原子采用
sp3
sp3
杂化,该分子的空间构型为三角锥形
三角锥形
,分子中N、H原子之间形成σ
σ
(填“σ”或“π”)键;已知W3+能与氨分子形成配离子[W(NH3)6]3+,该配离子中存在的化学键有
CD
CD
.(填标号)A.金属键 B.离子键 C.共价键 D.配位键.
[化学--物质结构与性质]
四种常见元素:A、B、C、D为周期表前四周期元素,原子序数依次递增,它们的性质或结构信息如下表.试根据信息回答有关问题.
(1)写出D原子的外围电子排布式
(2)B元素的氢化物的沸点比同主族相邻元素氢化物沸点
(3)元素F与A相邻且同主族,它们与氧元素的成键情况如下:
在A和O之间通过双键形成AO2分子,而F和O则不能和A那样形成有限分子,原因是
(4)往D元素的硫酸盐溶液中逐滴加入过量B元素的氢化物水溶液,可生成的配合物,该配合物中不含有的化学键是
(5)下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键.
”表示没有形成共价键的最外层电子,短线表示共价键.


则在以上分子中,中心原子采用sp3杂化形成化学键的是
(6)已知一种分子B4分子结构如图所示,断裂1molB-B吸收aKJ的热量,生成1molB≡B放出bKJ热量.试计算反应:B4(g)═2B2(g)△H=
查看习题详情和答案>>
四种常见元素:A、B、C、D为周期表前四周期元素,原子序数依次递增,它们的性质或结构信息如下表.试根据信息回答有关问题.
| 元素 | A | B | C | D |
| 结构性质 信息 |
基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 | 原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有2对成对的p电子 | 其原子序数比A、B、C三种元素原子的质子数总和还少1,有+1、+2两种常见化合价 |
3d104s1
3d104s1
,A、B、C、D四种元素的第一电离能最小的是Cu
Cu
(用元素符号表示).(2)B元素的氢化物的沸点比同主族相邻元素氢化物沸点
高
高
(填“高”或“低”).(3)元素F与A相邻且同主族,它们与氧元素的成键情况如下:
| A-O | A=O | F-O | F=O | |
| 键能(KJ/mol) | 360 | 803 | 464 | 640 |
C=O的键能比C-O的键能的两倍要大,Si=O的键能比Si-O的键能的两倍要小,所以Si和O成单键更稳定,而C和O以双键形成稳定分子
C=O的键能比C-O的键能的两倍要大,Si=O的键能比Si-O的键能的两倍要小,所以Si和O成单键更稳定,而C和O以双键形成稳定分子
.(4)往D元素的硫酸盐溶液中逐滴加入过量B元素的氢化物水溶液,可生成的配合物,该配合物中不含有的化学键是
ce
ce
(填序号).a.离子键 b.极性键c.非极性键d.配位键 e.金属键(5)下列分子结构图中的“
 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键.
”表示没有形成共价键的最外层电子,短线表示共价键.

则在以上分子中,中心原子采用sp3杂化形成化学键的是
①③
①③
(填序号);在②的分子中有3
3
个σ键和2
2
个π键.(6)已知一种分子B4分子结构如图所示,断裂1molB-B吸收aKJ的热量,生成1molB≡B放出bKJ热量.试计算反应:B4(g)═2B2(g)△H=
-(2b-6a)
-(2b-6a)
KJ/mol.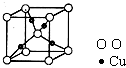 [化学--物质结构与性质]
[化学--物质结构与性质]第4周期过渡金属元素能形成多种多样的配合物.CO可以和过渡金属形成配合物.
(1)Fe3+离子的电子排布式为
1s22s22p63s23p63d5
1s22s22p63s23p63d5
.配合物Fe(CO)5的配位体是CO
CO
.常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂,熔点为251K,沸点为376K,据此,可判断Fe(CO)5晶体属于分子
分子
晶体(填“离子”、“原子”、“分子”或“金属”).CO和N2的价电子总数相同,CO和N2相似,分子中都存在一个共价叁键,其中包含1
1
个δ键,2
2
个π键.(2)一般地说,第4周期元素的第一电离能随原子序数的增大而增大,而31Ga的第一电离能却明显低于30Zn,原因是
Zn原子的价电子排布式为3d104s2,体系的能量较低,原子较稳定,故Zn的第一电离能大于Ga
Zn原子的价电子排布式为3d104s2,体系的能量较低,原子较稳定,故Zn的第一电离能大于Ga
.(3)下表为CO和N2的有关信息.根据表中数据,说明CO比N2活泼的原因:
CO中第一个π键的键能比N2的第一个π键的键能小很多,CO的第一个π键容易断裂
CO中第一个π键的键能比N2的第一个π键的键能小很多,CO的第一个π键容易断裂
.| 化学键 | C-O | C═O | C≡O |
| 键能(kJ/mol) | 351 | 803 | 1071 |
| 化学能 | N-N | N═N | N≡N |
| 键能(kj/mol) | 159 | 418 | 945 |
4
4
.[化学-物质结构与性质]

Ⅰ.短周期某主族元素M的电离能如图(A)所示.则M元素位于周期表的第
Ⅱ.图B折线c可以表达出第
Ⅲ.氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.
(1)写出这三种元素电负性由大到小的顺序
(2)砷原子核外电子排布式为
(3)K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键类型为
查看习题详情和答案>>

Ⅰ.短周期某主族元素M的电离能如图(A)所示.则M元素位于周期表的第
ⅡA
ⅡA
族.Ⅱ.图B折线c可以表达出第
IVA
IVA
族元素氢化物的沸点的变化规律.两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:b
b
(填“a”或“b”)Ⅲ.氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.
(1)写出这三种元素电负性由大到小的顺序
N>P>As
N>P>As
(填元素符号)(2)砷原子核外电子排布式为
1s22s22p63s23p63d104s24p3
1s22s22p63s23p63d104s24p3
(3)K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键类型为
配位键
配位键
,该化学 键能够形成的原因是CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道)
CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道)
.