摘要:10.在一密闭容器中.进行mX,△H<0的反应.下列说法正确的是 ( ) A.加入催化剂可以提高X的转化率 B.缩小容器的体积.混合体系中X的含量增加.则m一定小于3 C.降低温度.正反应速率增大.逆反应速率减小.混合体系中Z的含量增大 D.加入一些Y.平衡向右移动.可以提高X的转化率
网址:http://m.1010jiajiao.com/timu_id_1724203[举报]
在一密闭容器中,进行mX(g)+nY(s) ![]() 3Z(g);△H<0的反应,下列说法正确的是( )
3Z(g);△H<0的反应,下列说法正确的是( )
A.加入催化剂可以提高X的转化率
B.缩小容器的体积,混合体系中X的含量增加,则m一定小于3
C.降低温度,正反应速率增大,逆反应速率减小,混合体系中Z的含量增大
D.加入一些Y,平衡向右移动,可以提高X的转化率
查看习题详情和答案>>
在一密闭容器中,反应mX(g) nY(g)达到平衡之后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,X的浓度变为原来的60%,则下列说法不正确的是( )
nY(g)达到平衡之后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,X的浓度变为原来的60%,则下列说法不正确的是( )
A.平衡向正反应方向移动了 B.平衡向逆反应方向移动了
C.物质Y的质量分数减少了 D.m>n
查看习题详情和答案>>在一密闭容器中,进行mX(s)+nY(g)![]() 2Z(g);ΔH=Q的反应中,下列结论正确的是( )
2Z(g);ΔH=Q的反应中,下列结论正确的是( )
A.缩小容器的体积,发现混合气体的密度增大,则n一定大于2
B.加入一些X,平衡一定往右移动,可以提高Y的转化率
C.升高温度,正反应、逆反应速率同时增大,X和Y的质量增加,说明Q>0
D.若增大压强,Z的百分含量不变,则m+n>2
查看习题详情和答案>>
(2013?德州模拟)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
(1)在一密闭容器中,进行如下化学反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其化学平衡常数K与温度T的关系如下表:
①比较K1、K2的大小:K1
②若保持容器的容积不变,则该反应达到化学平衡状态的依据是
a.υ(N2)正=3υ(H2)逆
b.容器内N2、H2、NH3的浓度之比为1:3:2
c.容器内压强保持不变
d.混合气体的平均相对分子质量保持不变
(2)298K时,1.00g N2H4(l)与足量的N2O4(l)完全反应生成氮气和液态水,放出19.15kJ的热量.写出该反应的热化学方程式
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用[Cu(NH3)2]Ac溶液来吸收原料气中的CO,其反应是:
[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3]Ac?C
<0
生产中必须除去原料气中CO的原因是
(4)对反应2NO2(g)?N2O4(g)△H<0在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是
a.A、C两点的反应速率:A>C
b.A、C两点NO2的转化率:A<C
c.B、C两点的气体的平均相对分子质量:B<C
d.由状态B到状态A,可以用加热的方法.
查看习题详情和答案>>
(1)在一密闭容器中,进行如下化学反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其化学平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| K | 4.1×106 | K1 | K2 |
>
>
K2填“>”、“=”或“<”);②若保持容器的容积不变,则该反应达到化学平衡状态的依据是
cd
cd
(填序号).a.υ(N2)正=3υ(H2)逆
b.容器内N2、H2、NH3的浓度之比为1:3:2
c.容器内压强保持不变
d.混合气体的平均相对分子质量保持不变
(2)298K时,1.00g N2H4(l)与足量的N2O4(l)完全反应生成氮气和液态水,放出19.15kJ的热量.写出该反应的热化学方程式
2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)△H=-1225.6KJ/mol
2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)△H=-1225.6KJ/mol
;(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用[Cu(NH3)2]Ac溶液来吸收原料气中的CO,其反应是:

[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3]Ac?C
| O |
生产中必须除去原料气中CO的原因是
防止催化剂中毒
防止催化剂中毒
;[Cu(NH3)2]Ac溶液吸收原料气中CO的适宜条件应是低温高压
低温高压
.(4)对反应2NO2(g)?N2O4(g)△H<0在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是
bd
bd
(填字母序号).a.A、C两点的反应速率:A>C
b.A、C两点NO2的转化率:A<C
c.B、C两点的气体的平均相对分子质量:B<C
d.由状态B到状态A,可以用加热的方法.
氮元素有着多变价态和种类繁多的化合物,它们在工农业生产、生活中发挥着重要的作用.完成下列问题:
(1)在一密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其化学平衡常数K与温度T的关系如下表:
①比较K1、K2的大小:K1
②若保持容器的容积不变,则该反应达到化学平衡状态的依据是
a.2v正(H2)=3v逆(NH3) b.v正(N2)=3v逆(H2)
c.容器内压强保持不变 d.混合气体的平均摩尔质量保持不变
③若维持容器的体积不变,达到平衡状态后再向容器中通入一定量的N2,此时逆反应速率
④已知AgCl可溶于氨水中,而AgBr不溶于氨水中,则Ksp(AgCl)
(2)肼是氮元素的另一种氢化物,分子式为N2H4.
①写出肼的电子式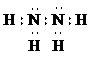
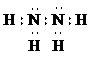 ,它属于
,它属于
②298K时,1.00g N2H4(l)与足量的N2O4(l)完全反应生成氮气和水,放出19.15kJ的热量.写该反应的热化学方程式
③肼也可以在纯氧中燃烧生成氮气和水,为了充分利用其能量有人设计了原电池装置,电极材料是多孔石墨电极,电解质为能够传导H+的固体电解质,请写出负极反应式
查看习题详情和答案>>
(1)在一密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其化学平衡常数K与温度T的关系如下表:
| T | 298K | 398K | 498K | … |
| K | 4.1×106 | K1 | K2 | … |
>
>
K2(填“>”、“=”或“<”).②若保持容器的容积不变,则该反应达到化学平衡状态的依据是
acd
acd
(填序号).a.2v正(H2)=3v逆(NH3) b.v正(N2)=3v逆(H2)
c.容器内压强保持不变 d.混合气体的平均摩尔质量保持不变
③若维持容器的体积不变,达到平衡状态后再向容器中通入一定量的N2,此时逆反应速率
不变
不变
(填“增大”、“减小”或“不变”);平衡向正反应
正反应
方向移动.④已知AgCl可溶于氨水中,而AgBr不溶于氨水中,则Ksp(AgCl)
>
>
Ksp(AgBr).(2)肼是氮元素的另一种氢化物,分子式为N2H4.
①写出肼的电子式
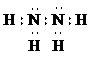
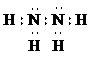
极
极
性分子.②298K时,1.00g N2H4(l)与足量的N2O4(l)完全反应生成氮气和水,放出19.15kJ的热量.写该反应的热化学方程式
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1225.6 kJ/mol
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1225.6 kJ/mol
.③肼也可以在纯氧中燃烧生成氮气和水,为了充分利用其能量有人设计了原电池装置,电极材料是多孔石墨电极,电解质为能够传导H+的固体电解质,请写出负极反应式
N2H4-4e-═N2+4H+
N2H4-4e-═N2+4H+
.