摘要:18.人体血液里Ca2+的浓度一般采用g·L-1表示.今抽一血样20.00mL.加适量的草酸铵[(NH4)2C204]溶液.可析出草酸钙(CaC204.)沉淀.将此沉淀过滤洗涤后溶于稀硫酸可得草酸.再用0.002 KMnO4.溶液滴定.使草酸转化成CO2逸出.反应的离子方程式为:5H2C204+2MnO4-+6H+===2Mn2++10C02↑+8H2O. (1)滴定时.KMnO4溶液应装在右图中的 滴定管中.操作时.左手 .右手 . (2)滴定时.根据现象 ,即可确定反应达到终点.因此.不必另外再加指示剂 (3)若滴定开始和结束时.酸式滴定管中的液面如图所示:则起始读数为 mL.终点读数为 mL 经过计算.血液样品中Ca2+的浓度为 g·L-1. (4)下列操作中可能使所测血液里Ca2+的浓度数值偏低的是 A.滴定管未用标准KMnO4溶液润洗.就直接注入标准KMn04溶液 B.滴定前盛放草酸溶液的锥形瓶用蒸馏水洗净后没有干燥 C.酸式滴定管在滴定前有气泡.滴定后气泡消失 D.读取KMnO4溶液体积时.开始仰视读数.滴定结束时俯视读数 E.滴定过程中.锥形瓶的振荡过于激烈.使少量溶液溅出 F.将锥形瓶用待测液润洗.然后加入待测液.再进行滴定
网址:http://m.1010jiajiao.com/timu_id_1724145[举报]
人体血液里Ca2+的浓度一般采用mg/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度.
配制KMnO4标准溶液如图所示是配制50mL KMnO4 标准溶液的过程示意图.

(1)请你观察图示判断,其中不正确的操作有(填序号)
(2)其中确定50mL溶液体积的容器是(填名称)
(3)如果用图示的操作配制溶液,所配制的溶液浓度将
测定血液样品中Ca2+的浓度:抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L KMnO4 溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液.
(4)已知草酸跟KMnO4反应的离子方程式为:2MnO
+5H2C2O4+6H+═2Mnx++10CO2↑+8H2O
则方程式中的x=
(5)经过计算,血液样品中Ca2+的浓度为
查看习题详情和答案>>
配制KMnO4标准溶液如图所示是配制50mL KMnO4 标准溶液的过程示意图.

(1)请你观察图示判断,其中不正确的操作有(填序号)
②⑤
②⑤
;(2)其中确定50mL溶液体积的容器是(填名称)
容量瓶
容量瓶
;(3)如果用图示的操作配制溶液,所配制的溶液浓度将
偏小
偏小
(填“偏大”或“偏小”).测定血液样品中Ca2+的浓度:抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L KMnO4 溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液.
(4)已知草酸跟KMnO4反应的离子方程式为:2MnO
- 4 |
则方程式中的x=
2
2
.(5)经过计算,血液样品中Ca2+的浓度为
1.2
1.2
mg/cm3.人体血液里Ca2+的浓度一般采用g/cm3来表示(即1 cm3血样中含有的Ca2+的质量)。抽取 一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得弱酸草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
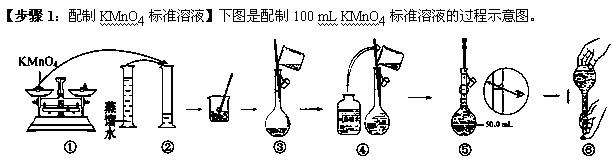 (1)请你观察图示判断,其中不正确的两项操作有 (填序号);
(1)请你观察图示判断,其中不正确的两项操作有 (填序号);
(2)其中确定100 mL溶液体积的仪器是__________________
(3)如果用图示的操作所配制的溶液进行实验,在其他操作正确的情况下,所配制的溶液浓度将
______(填“偏大”或“偏小”)。
【步骤2:测定血液样品中Ca2+的浓度】抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L 酸性KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)写出草酸与酸性KMnO4溶液反应的离子方程式 。
(5)滴定的终点为 。
(6)经过计算,血液样品中Ca2+的浓度为__________g/cm3。
查看习题详情和答案>>人的血液里Ca2+的浓度一般采用g·cm-3表示,今抽一血样20.00 mL加入适量的草酸铵[(NH4)2C2O4]溶液,可析出CaC2O4沉淀,将沉淀冼净后溶于强酸可得草酸,再用浓度为0.02 mol·L-1的KMnO4溶液滴定。当观察到溶液紫色褪尽时,共消耗12.00 mL KMnO4溶液。则该血液样品中Ca2+的浓度为( )
- A.0.0015 g·cm-3
- B.0.0012 g·cm-3
- C.0.0024 g·cm-3
- D.0.002 g·cm-3