网址:http://m.1010jiajiao.com/timu_id_1724102[举报]
 (2009?三明一模)张明同学在学习“硫酸及其盐的某些性质与用途“中,进行如下实验探究.
(2009?三明一模)张明同学在学习“硫酸及其盐的某些性质与用途“中,进行如下实验探究.[实验一]探究浓硫酸的氧化性
将实验室常用的药品放入如图所示的实验装置后,加热装置甲.(夹持和加热装置省略)
(1)该装置设计上存在明显缺陷,请指出:
(2)写出装置甲中反应的化学方程式:
| ||
| ||
| ||
| ||
(3)装置乙中的试剂是
[实验二]探究某硫酸亚铁盐固体是否变质
(4)请你帮助张明同学完成如下实验方案:
| 实验操作 | 预期现象和结论 |
往一支试管中加入少量固体,加水溶解,再滴加几滴KSCN溶液 往一支试管中加入少量固体,加水溶解,再滴加几滴KSCN溶液 |
若溶液变为红色,说明该固体已变质;若溶液未变红色,说明该固体没有变质 若溶液变为红色,说明该固体已变质;若溶液未变红色,说明该固体没有变质 |
查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,示意图如下:

张明用此法制取一定浓度的H2O2,并进行下列实验测定H2O2的质量分数:(离子方程式:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑)
①取5.00mL H2O2溶液(密度为1.00g/mL)置于锥形瓶中加水稀释,再加稀硫酸酸化;
②用0.1000mol/L KMnO4溶液滴定;
③用同样方法滴定,三次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL.
回答下列问题:
(5)电解饱和KHSO4溶液时,阳极的电极反应式为
(6)操作②中,滴入第一滴KMnO4溶液,溶液紫红色消失很慢,随着滴定过程中Mn2+的增多,溶液紫红色消失速率加快.Mn2+的作用是
(7)原H2O2溶液中溶质的质量分数为
某混合碱是①Na2CO3和NaHCO3或②Na2CO3和NaOH.用“双指示剂法”对样品的组分和总碱量[n(Na2O)]进行测定.实验方案:称取0.2960 g样品配成500 mL溶液,取25.00 mL置于250 mL锥形瓶中,加适量蒸馏水和几滴酚酞,用0.0100 mol·L-1的盐酸标准溶液将混合碱滴定成NaHCO3,然后再用溴甲酚绿——二甲基黄为指示剂进行滴定,将NaHCO3完全中和.
(1)某同学平行滴定了三次,每次滴定从"0点开始读数,其中第Ⅰ次滴定的第一个终点的液面如图所示,请读出实验数据,填入下列表格中


(2)该混合碱样品的组成为________,理由________.
(3)将混合碱滴定成NaHCO3的过程中,为了结果更加准确,应始终逐滴滴加,这样操作的原因是________.
(4)上述碱样中总碱量[n(Na2O)]是多少?写出计算过程________.
(5)如果本实验只测定样品的总碱量,实验方案应该怎样设计:________.
某混合碱是①Na2CO3和NaHCO3或②Na2CO3和NaOH.用“双指示剂法”对样品的组分和总碱量[n(Na2O)]进行测定.实验方案:称取0.2960 g样品配成500 mL溶液,取25.00 mL置于250 mL锥形瓶中,加适量蒸馆水和几滴酚酞,用0.0100 mol·L-1的盐酸标准溶液将混合碱滴定成NaHCO3,然后再用溴甲酚绿——二甲基黄为指示剂进行滴定,将NaHCO3完全中和.
(1)某同学平行滴定了三次,每次滴定从"0"点开始读数,其中第Ⅰ次滴定的第一个终点的液面如下图所示,请读出实验数据,填入下列表格中


(2)该混合碱样品的组成为________,理由_________________.
(3)将混合碱滴定成NaHCO3的过程中,为了结果更加准确,应始终逐滴滴加,这样操作的原因是________.
(4)上述碱样中总碱量[n(Na2O)]是多少?写出计算过程________.
(5)如果本实验只测定样品的总碱量,实验方案应该怎样设计:________.
用稀H2SO4、NaOH溶液和废铝为原料制取Al(OH)3,甲、乙、丙三位同学的制备途径如下,请对此回答问题:
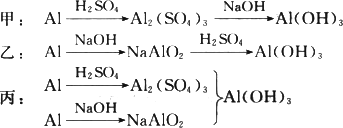
(1)在三个方案中,其中有一个的化学变化里涉及到两种盐在溶液中发生反应,写出该化学反应的离子方程式:________.
(2)从获得同样多的产品而原料用量最少的角度来看,三个方案中最理想的是________.在你认为不够理想的方案中,除去原料消耗量的因素以外,还有方案不理想的理由是(任选一个方案谈一个主要理由)________.
(3)在你认为理想的方案中,为了达到使一定质量的废铝充分利用的目的,在方案实施之前,还要做的定量实验是________.
(一)补全以下检验混合物中存在K2CO3的实验步骤及相关现象
1.取混合物样品溶于水,分别取少量溶液进行以下实验
2._________________________________________则一定存在K+;
3.___________________________________________________则一定存在CO32—。
(二)测定K2CO3质量分数
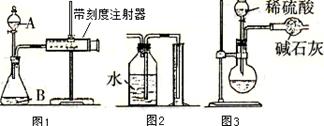
(1)甲同学用图1所示装置,把xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是
。
(2)乙同学用图2代替图1中的收集装置,则所测K2CO3质量分数 (填“偏大”、“偏小”、“不变”),你的改进方案是 。
(3)丙同学用图3装置测定CO2的质量,该装置存在较多缺陷,从而导致实验误差,请你填写其中的三点缺陷:I ;
Ⅱ
Ⅲ