摘要:31.[化学-化学与技术] 海水中镁的总储量约为2.1×15t.目前世界上的60%的镁来自海水.工业规模海水提镁的流程如图所示: 试回答下列问题: (1)请写出海水提镁的过程中①②反应的化学方程式:① , ② . (2)工业上采用电解MgCl2的方法制得金属镁.电解槽中阴极的电极反应式为: . (3)工业上制取金属铝时不用电解AlCl3的方法而是用电解熔融Al2O3的方法.试解释铝电解槽中的阳极碳块为何要定期更换? .
网址:http://m.1010jiajiao.com/timu_id_1724052[举报]
[化学--化学与技术]
海水中镁的总储量约为2.1×1015t,目前世界上的60%的镁来自海水.工业规模海水提镁的流程(如图所示),其步骤为:①将海水中大量存在的贝壳煅烧成石灰;②将石灰制成石灰乳;③将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;④在Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O;⑤将MgCl2?6H2O在一定条件下加热得到无水MgCl2;⑥电解熔融的MgCl2可得到镁.

试回答下列问题:
(1)请写出海水提镁的过程中①⑥反应的化学方程式:
① ; ⑥ .
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为: ;
(3)步骤④中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有 、 、 、 、铁架台等;
(4)步骤⑤中的“一定条件”指的是 目的是
(5)上述制镁的流程中,可以在降低成本,减少污染方面做出一些工作,请写出其中一点 ;
(6)有同学认为上述过程中,可加热Mg(OH)2得到MgO,再电解熔融MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则.你同意该同学的想法吗?为什么? .
查看习题详情和答案>>
海水中镁的总储量约为2.1×1015t,目前世界上的60%的镁来自海水.工业规模海水提镁的流程(如图所示),其步骤为:①将海水中大量存在的贝壳煅烧成石灰;②将石灰制成石灰乳;③将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;④在Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O;⑤将MgCl2?6H2O在一定条件下加热得到无水MgCl2;⑥电解熔融的MgCl2可得到镁.

试回答下列问题:
(1)请写出海水提镁的过程中①⑥反应的化学方程式:
①
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为:
(3)步骤④中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有
(4)步骤⑤中的“一定条件”指的是
(5)上述制镁的流程中,可以在降低成本,减少污染方面做出一些工作,请写出其中一点
(6)有同学认为上述过程中,可加热Mg(OH)2得到MgO,再电解熔融MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则.你同意该同学的想法吗?为什么?
(三选一)[选修2:化学与技术]
海水是巨大的资源宝库,溴的提取就是以海水为原料,其提取工艺流程如下图:
海水是巨大的资源宝库,溴的提取就是以海水为原料,其提取工艺流程如下图:

(1)请列举两种海水淡化的方法__________
(2)步骤③反应的化学方程式是______________________________
(3)步骤⑤蒸馏的过程中,温度应控制在80~90℃,温度过高或过低都不利于生产,请解释原因_________________________________
(4)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏,得到液溴?_________________。
查看习题详情和答案>>
(2)步骤③反应的化学方程式是______________________________
(3)步骤⑤蒸馏的过程中,温度应控制在80~90℃,温度过高或过低都不利于生产,请解释原因_________________________________
(4)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏,得到液溴?_________________。
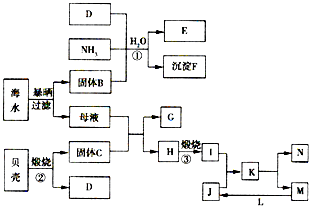 [化学与技术]海洋是巨大的资源宝库,从海洋中我们可以获得各种各样的化学物质,下图是综合利用海洋资源的一个例子(假设海水中存在的离子主要有Na+、Mg2+、Cl-).
[化学与技术]海洋是巨大的资源宝库,从海洋中我们可以获得各种各样的化学物质,下图是综合利用海洋资源的一个例子(假设海水中存在的离子主要有Na+、Mg2+、Cl-).(1)反应①是著名的侯氏制碱法生产原理中的重要反应,其化学反应方程式是
NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
.实际生产中,在固体B的溶液中是先通入D气体还是先通入NH3?
先通入NH3
先通入NH3
.(2)对固体B精制后,用惰性电极电解其水溶液,阴极的电极反应式为
2H++2e-=H2↑
2H++2e-=H2↑
.(3)在上述转化关系中,电解熔融态的K可制得一种常见的金属N.写出该反应的化学方程式
MgCl2
Mg+Cl2↑
| ||
MgCl2
Mg+Cl2↑
.
| ||
(4)由K溶液经如何处理才能制得N?
MgCl2溶液要在HCl气体氛围中进行蒸发结晶制得MgCl2晶体,熔融后电解才能制取金属镁
MgCl2溶液要在HCl气体氛围中进行蒸发结晶制得MgCl2晶体,熔融后电解才能制取金属镁
.(2011?怀化一模)化学一化学与技术
我国有丰富的天然气资源.以天然气为原料合成尿素的主要流程如图所示(图中某些转化步骤及生成物未列出)
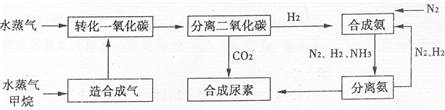
请填写下列空白:
(1)合成尿素的反应分二步,请写出该反应的化学方程式
①
②
(2)依据流程圈,判断下列说法正确的是
A.在转化CO的过程中使用催化剂,可以提高CO的转化率
B.进入分离二氧化碳装置的气体有2种
C.N2、H2的循环使用,提高了原子的利用率
D.二氧化碳与氨合成尿素属于人工固氮
E.流程中的原料有3种取之不尽,用之不完
(3)合成氨选择的外界条件是:催化剂,20~50MPa的压强,500℃的温度.选择该温度的主要原因是
(4)已知制造合成气的反应为CH4(g)+H2O(g)?CO(g)+3H2(g),该反应的平衡常数表达式为K=
.降低温度K减小,则正反应是一个
查看习题详情和答案>>
我国有丰富的天然气资源.以天然气为原料合成尿素的主要流程如图所示(图中某些转化步骤及生成物未列出)

请填写下列空白:
(1)合成尿素的反应分二步,请写出该反应的化学方程式
①
2NH3+CO2
NH2COONH4
| ||
2NH3+CO2
NH2COONH4
;
| ||
②
NH2COONH4
CO(NH2)2+H2O
| ||
NH2COONH4
CO(NH2)2+H2O
.
| ||
(2)依据流程圈,判断下列说法正确的是
C
C
.A.在转化CO的过程中使用催化剂,可以提高CO的转化率
B.进入分离二氧化碳装置的气体有2种
C.N2、H2的循环使用,提高了原子的利用率
D.二氧化碳与氨合成尿素属于人工固氮
E.流程中的原料有3种取之不尽,用之不完
(3)合成氨选择的外界条件是:催化剂,20~50MPa的压强,500℃的温度.选择该温度的主要原因是
500℃的温度反应速率较快,催化剂活性最高
500℃的温度反应速率较快,催化剂活性最高
.(4)已知制造合成气的反应为CH4(g)+H2O(g)?CO(g)+3H2(g),该反应的平衡常数表达式为K=
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
吸
吸
热反应.当造合成气的反应中甲烷的转化率为75%.合成氨中氢气的转化率为40%(其他过程的损失不计)以5.60xlO7L甲烷为原料能够合成4.48xlO7L
4.48xlO7L
L氨气.(假设体积均在标准状况下测定)【化学-选修化学与技术】
海水中镁的总储量约为2.1×1015 t,目前世界生产的镁60%来自海水.海水的综合利用可以制备金属镁,其流程如下图所示:

其步骤为:
①将海边大量存在的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
②将石灰乳加入到经过蒸发浓缩并滤去粗盐后的海水中,过滤得到Mg(OH)2沉淀;
③向Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O;
④将MgCl2?6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的MgCl2可得到Mg.
请回答下列问题:
(1)步骤①中煅烧贝壳时所发生反应的化学方程式为 .
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为 .
(3)步骤③中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有 、 、酒精灯、铁架台等.
(4)海水中的镁以Mg2+的形式存在,设计步骤②③将Mg2+转化为Mg(OH)2,然后又重新转化为Mg2+的目的是 .
(5)步骤④中的“一定条件”指的是 ,目的是 .
(6)在上述制取镁的流程中,所涉及到的基本反应类型有 .
a.化和反应b.分解反应c.置换反应d.复分解反应
(7)由海水得到的粗盐中常含有Ca2+、Mg2+、SO42-等杂质,为除去这些杂质可加入Na2CO3、NaOH和BaCl2,然后过滤,则所加入试剂的合理顺序为 .
查看习题详情和答案>>
海水中镁的总储量约为2.1×1015 t,目前世界生产的镁60%来自海水.海水的综合利用可以制备金属镁,其流程如下图所示:

其步骤为:
①将海边大量存在的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
②将石灰乳加入到经过蒸发浓缩并滤去粗盐后的海水中,过滤得到Mg(OH)2沉淀;
③向Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O;
④将MgCl2?6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的MgCl2可得到Mg.
请回答下列问题:
(1)步骤①中煅烧贝壳时所发生反应的化学方程式为
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为
(3)步骤③中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有
(4)海水中的镁以Mg2+的形式存在,设计步骤②③将Mg2+转化为Mg(OH)2,然后又重新转化为Mg2+的目的是
(5)步骤④中的“一定条件”指的是
(6)在上述制取镁的流程中,所涉及到的基本反应类型有
a.化和反应b.分解反应c.置换反应d.复分解反应
(7)由海水得到的粗盐中常含有Ca2+、Mg2+、SO42-等杂质,为除去这些杂质可加入Na2CO3、NaOH和BaCl2,然后过滤,则所加入试剂的合理顺序为