网址:http://m.1010jiajiao.com/timu_id_1723979[举报]
氢酸一种强酸,氯酸溶液浓度若超过40%就会迅速分解,产生一种酸性比它更强的酸,同时放出气体,该混合气体干燥后的平均相对分子质量为45,它可以使带有火星的木条复燃,又可以使湿润的淀粉碘化钾试纸变蓝后又褪色,试写出:
(1)气体与湿润的淀粉碘化钾试纸发生反应的离子方程式。
。
(2)氯酸分解的化学方程式:
。
(3)生成1mol更强酸时,转移电子的物质的量是 mol,生成气体在标准状况下的体积为 L。
查看习题详情和答案>>亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,在碱性溶液中NaClO2比较稳定,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
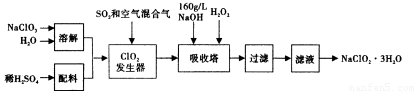
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 g NaOH固体溶于水所得溶液的体积为1L。
(1)160 g/L NaOH溶液的物质的量浓度为____。若要计算该溶液的质量分数,还需要的一个条件是____(用文字说明)。
(2)发生器中鼓入空气的作用可能是____(选填序号)。
a.将SO2氧化成SO3,增强酸性;
b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为____。吸收塔的温度不能超过20℃,其目的是 。
(4)吸收塔中应维持NaOH稍过量,理由是____。
(5)吸收塔中能否用FeCl2代替H2O2____(填能.否)?理由是____。
(6)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是____(选填序号)。
A.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2·3H2O晶体必须进行的操作是____(填操作名称)。
查看习题详情和答案>>
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,在碱性溶液中NaClO2比较稳定,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图: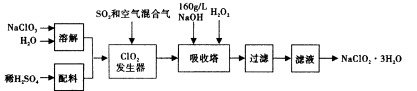
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 g NaOH固体溶于水所得溶液的体积为1L。
(1)160 g/L NaOH溶液的物质的量浓度为____。若要计算该溶液的质量分数,还需要的一个条件是____(用文字说明)。
(2)发生器中鼓入空气的作用可能是____(选填序号)。
a.将SO2氧化成SO3,增强酸性;
b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为____。吸收塔的温度不能超过20℃,其目的是 。
(4)吸收塔中应维持NaOH稍过量,理由是____。
(5)吸收塔中能否用FeCl2代替H2O2____(填能.否)?理由是____。
(6)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是____(选填序号)。
A.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2·3H2O晶体必须进行的操作是____(填操作名称)。

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 g NaOH固体溶于水所得溶液的体积为1L。
(1)160 g/L NaOH溶液的物质的量浓度为____。若要计算该溶液的质量分数,还需要的一个条件是____(用文字说明)。
(2)发生器中鼓入空气的作用可能是____(选填序号)。
a.将SO2氧化成SO3,增强酸性;
b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为____。吸收塔的温度不能超过20℃,其目的是 。
(4)吸收塔中应维持NaOH稍过量,理由是____。
(5)吸收塔中能否用FeCl2代替H2O2____(填能.否)?理由是____。
(6)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是____(选填序号)。
A.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2·3H2O晶体必须进行的操作是____(填操作名称)。
 (10分)I 实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:
(10分)I 实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:
⑴用硝酸溶解大理石时通常控制反应温度不超过70℃,且不使用浓硝酸,原因是
、 。
⑵操作Ⅱ的目的是 , 若A为溶液,则A可以是 。
⑶写出加入碳酸铵所发生反应的离子方程式: 。
II 以硫酸工业的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCl为原料可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下:

⑷已知对苯二酚是一种强还原剂。生产中,反应Ⅱ中往往需要向溶液中加入适量的对苯二酚等物质,其目的是 。
⑸下列有关说法正确的是 。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅲ中发生反应的化学方程式为:CaSO4+4C![]() CaS +4CO↑
CaS +4CO↑
C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
⑹反应Ⅴ反应液用40%乙二醇溶液,温度控制在25℃,硫酸钾的产率超过90%,其原因是
。
⑺(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为N2,试写出二氧化氮与亚硫酸铵反应的化学方程式 。
查看习题详情和答案>>