摘要:19.加入0.1 mol MnO2粉末于50 mL过氧化氢(H2O2.ρ=1.1 g·mL-1)中.在标准状况下放出气体的体积和时间的关系如右图所示. (1)实验时放出气体的总体积是 .放出气体所需时间为 . (2)A.B.C.D各点反应速率快慢的顺序为 .解释反应速率变化的原因 . (3)计算H2O2的初始物质的量浓度 .
网址:http://m.1010jiajiao.com/timu_id_1723399[举报]
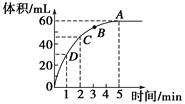
加入0.1 mol MnO2粉末于50 mL过氧化氢溶液(ρ=1.1 g·mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示。
(1)反应放出![]() 气体所需时间为_____________
气体所需时间为_____________
(2)A、B、C、D各点反应速率快慢的顺序为_____________
(3)计算H2O2的初始物质的量浓度_____________
(4)求反应到2 min时,H2O2的质量分数_____________

加入0.1 mol的MnO2粉末于50 mL过氧化氢的溶液中(密度为1.1 g ·mL-1),在标准状况下放出气体的体积和时间的关系如图2-7所示,完成下列问题:

图2-7
(1)实验时放出气体的总体积为_________________。
(2)放出一半气体所需要的时间为_________________。
(3)反应放出3/4气体所需要的时间为_________________。
(4)A、B、C、D四点化学反应速率快慢的顺序为_________________。
查看习题详情和答案>>
加入0.1 mol的MnO2粉末于50 mL过氧化氢的溶液中(密度为1.1 g ·mL-1),在标准状况下放出气体的体积和时间的关系如下图所示,请完成下列问题:

(1)实验时放出气体的总体积为______________。
(2)放出一半气体所需要的时间为______________。
(3)反应放出3/4气体所需要的时间为______________。
(4)A、B、C、D四点化学反应速率由快到慢的顺序为______________。
查看习题详情和答案>>