摘要:3.下列说法正确的是: A.HI的相对分子质量大于HF.所以HI的沸点高于HF B.由ⅠA和ⅥA族元素形成的原子个数比为1∶1.电子总数为38的化合物.是含有共价键的离子型化合物 C.H与D.16O与18O 互为同位素.H2.D2互为同素异形体 D.在SiO2 晶体中.1个Si原子和2个O原子形成2个共价键
网址:http://m.1010jiajiao.com/timu_id_1723282[举报]
|
下列说法正确的是: | |
| [ ] | |
A. |
HI的相对分子质量大于HF,所以HI的沸点高于HF |
B. |
由ⅠA和ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子型化合物 |
C. |
H与D、16O与18O互为同位素,H2、D2互为同素异形体 |
D. |
在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
若NA表示阿伏加德罗常数的值,下列说法不正确的是
[ ]
①C2H6分子中既含极性键又含非极性键
②若R2-和M+的电子层结构相同,则原子序数:R >M
③F2、Cl2、Br2、I2的熔点随相对分子质量增大而升高
④由于非金属性Cl>Br >I,所以酸性HCl>HBr> HI
⑤标准状况下,100 g含氢质量分数为12%的C2H4和甲醛的混合气体中氧原子数为NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2NA
⑦16.9 g过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA
A.②④⑥⑦
B.①③④⑤
C.②④⑤⑦
D.③⑤⑦
查看习题详情和答案>>
②若R2-和M+的电子层结构相同,则原子序数:R >M
③F2、Cl2、Br2、I2的熔点随相对分子质量增大而升高
④由于非金属性Cl>Br >I,所以酸性HCl>HBr> HI
⑤标准状况下,100 g含氢质量分数为12%的C2H4和甲醛的混合气体中氧原子数为NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2NA
⑦16.9 g过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA
A.②④⑥⑦
B.①③④⑤
C.②④⑤⑦
D.③⑤⑦
下表中的数据是破坏1 mol物质中的化学键所消耗的能量(kJ):

根据上述数据问题。
(1)下列物质本身具有的能量最低的是 _____(填序号)
A.H2 B.Cl2 C.Br2 D.I2
化合物HCl、HBr、HI中______受热时最稳定。
(2)1molH2在2mol Cl2中燃烧,放出热量________ kJ 。一定条件下,1mol H2分别与足量Cl2、Br2、I2反应,放出热量由多到少的顺序是________ (填序号)
A Cl2<Br2<I2 B Cl2>Br2>I2
(3)下列有关化学键及键参数的说法中正确的是__________(填序号)
① 原子或分子间的相互作用叫化学键
② 氯分子中两个氯原子间的距离是键长
③ 键长的大小与成键原子的半径和成键数目有关
④ 键角是描述分子立体结构的重要参数
(4)下列事实不能用键能的大小来解释的是___________(填序号)
A.乙炔比氮气均含三键但是前者比后者容易发生加成反应
B.N2、O2、F2跟氢气的反应能力依次增强
C.硝酸是挥发性酸,而硫酸、磷酸是难不挥发性酸
(5)氰气[(CN)2]无色、剧毒、有苦杏仁味,和卤素单质性质相似。
①写出(CN)2与苛性钠溶液反应的离子方程式______________________;
②已知氰分子中键与键之间的夹角为180.,并有对称性, 则结构式为_______
③氰分子中碳原子为_______杂化;一个氰分子中包含_______个σ键,____个键。
查看习题详情和答案>>
(1)下列物质本身具有的能量最低的是 _____(填序号)
A.H2 B.Cl2 C.Br2 D.I2
化合物HCl、HBr、HI中______受热时最稳定。
(2)1molH2在2mol Cl2中燃烧,放出热量________ kJ 。一定条件下,1mol H2分别与足量Cl2、Br2、I2反应,放出热量由多到少的顺序是________ (填序号)
A Cl2<Br2<I2 B Cl2>Br2>I2
(3)下列有关化学键及键参数的说法中正确的是__________(填序号)
① 原子或分子间的相互作用叫化学键
② 氯分子中两个氯原子间的距离是键长
③ 键长的大小与成键原子的半径和成键数目有关
④ 键角是描述分子立体结构的重要参数
(4)下列事实不能用键能的大小来解释的是___________(填序号)
A.乙炔比氮气均含三键但是前者比后者容易发生加成反应
B.N2、O2、F2跟氢气的反应能力依次增强
C.硝酸是挥发性酸,而硫酸、磷酸是难不挥发性酸
(5)氰气[(CN)2]无色、剧毒、有苦杏仁味,和卤素单质性质相似。
①写出(CN)2与苛性钠溶液反应的离子方程式______________________;
②已知氰分子中键与键之间的夹角为180.,并有对称性, 则结构式为_______
③氰分子中碳原子为_______杂化;一个氰分子中包含_______个σ键,____个键。
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数 (25℃) | 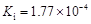 |  | 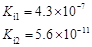 | 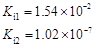 |
(1)在温度相同时,各弱酸的Ki值与酸性的相对强弱的关系为:________________________。
(2)下列离子方程式正确的是
A.2ClO- + H2O + CO2 → 2HClO + CO32-
B.2HCOOH + CO32- → 2HCOO- + H2O + CO2↑
C.H2SO3 + 2HCOO- → 2HCOOH + SO32-
D.Cl2 + H2O+2CO32- → 2HCO3- + Cl- + ClO-
(3)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为 。
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性。
(4)往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式: 。
(5)将亚硒酸与30%的H2O2加热可制得硒酸(H2SeO4),反应方程式如下:
H2SeO3 + H2O2 → H2SeO4+H2O,下列说法中正确的是…………………………………( )
A.H2O2既是氧化剂又是还原剂
B.H2O 既不是氧化产物又不是还原产物
C.H2SeO4既是氧化产物又是还原产物
D.氧化性:H2SeO3>H2SeO4
碲酸(H6TeO6)是一种很弱的酸,
 ,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:HI+ H6TeO6
 TeO2+ Te+ I2+ H2O
TeO2+ Te+ I2+ H2O(6)若反应中生成的TeO2与Te的物质的量之比为
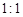 ,试配平上述化学方程式。
查看习题详情和答案>>
,试配平上述化学方程式。
查看习题详情和答案>>
部分弱酸的电离平衡常数如下表:
(1)在温度相同时,各弱酸的Ki值与酸性的相对强弱的关系为:________________________。
(2)下列离子方程式正确的是
A.2ClO- + H2O + CO2 → 2HClO + CO32-
B.2HCOOH + CO32- → 2HCOO- + H2O + CO2↑
C.H2SO3 + 2HCOO- → 2HCOOH + SO32-
D.Cl2 + H2O+2CO32- → 2HCO3- + Cl- + ClO-
(3)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为 。
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性。
(4)往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式: 。
(5)将亚硒酸与30%的H2O2加热可制得硒酸(H2SeO4),反应方程式如下:
H2SeO3 + H2O2 → H2SeO4+H2O,下列说法中正确的是…………………………………( )
A.H2O2既是氧化剂又是还原剂
B.H2O 既不是氧化产物又不是还原产物
C.H2SeO4既是氧化产物又是还原产物
D.氧化性:H2SeO3>H2SeO4
碲酸(H6TeO6)是一种很弱的酸,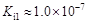 ,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
HI+ H6TeO6 TeO2+ Te+ I2+ H2O
TeO2+ Te+ I2+ H2O
(6)若反应中生成的TeO2与Te的物质的量之比为 ,试配平上述化学方程式。
,试配平上述化学方程式。
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数 (25℃) | 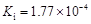 |  |  |  |
(1)在温度相同时,各弱酸的Ki值与酸性的相对强弱的关系为:________________________。
(2)下列离子方程式正确的是
A.2ClO- + H2O + CO2 → 2HClO + CO32-
B.2HCOOH + CO32- → 2HCOO- + H2O + CO2↑
C.H2SO3 + 2HCOO- → 2HCOOH + SO32-
D.Cl2 + H2O+2CO32- → 2HCO3- + Cl- + ClO-
(3)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为 。
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性。
(4)往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式: 。
(5)将亚硒酸与30%的H2O2加热可制得硒酸(H2SeO4),反应方程式如下:
H2SeO3 + H2O2 → H2SeO4+H2O,下列说法中正确的是…………………………………( )
A.H2O2既是氧化剂又是还原剂
B.H2O 既不是氧化产物又不是还原产物
C.H2SeO4既是氧化产物又是还原产物
D.氧化性:H2SeO3>H2SeO4
碲酸(H6TeO6)是一种很弱的酸,
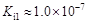 ,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:HI+ H6TeO6
 TeO2+ Te+ I2+ H2O
TeO2+ Te+ I2+ H2O(6)若反应中生成的TeO2与Te的物质的量之比为
 ,试配平上述化学方程式。
,试配平上述化学方程式。