摘要:7.若ⅢA族某元素的原子序数为m.则原子序数为m – 1的元素 ( ) A.一定是第ⅡA族元素 B.一定是第ⅡB族元素 C.可能是第ⅡA族或第ⅡB族元素 D.可能是第ⅤⅢ族元素
网址:http://m.1010jiajiao.com/timu_id_1722130[举报]
现有部分短周期元素的性质或原子结构如下表:
(1)用化学用语回答下列问题:
①A元素在周期表中的位置
②B元素原子结构示意图
 ;
;
③C单质分子的电子式
 ;用电子式表示A和B元素组成的化合物的形成过程
;用电子式表示A和B元素组成的化合物的形成过程
 ;
;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素
(2)元素D与元素A相比,非金属性较强的是
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下列过程转化为W(其他条件略去).
X
Y
Z
W.
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:
查看习题详情和答案>>
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
①A元素在周期表中的位置
第三周期ⅥA族
第三周期ⅥA族
;②B元素原子结构示意图


③C单质分子的电子式




④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素
1737Cl
1737Cl
.(2)元素D与元素A相比,非金属性较强的是
Cl
Cl
(用元素符号表示),下列表述中能证明这一事实的是bde
bde
(填选项序号).a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是
NaOH
NaOH
(写化学式).(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下列过程转化为W(其他条件略去).
X
| O2 |
| O2 |
| H2O |
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为:
BaSO4
BaSO4
;生成该白色沉淀的化学方程式为BaCl2+SO2+H2O2=BaSO4↓+2HCl
BaCl2+SO2+H2O2=BaSO4↓+2HCl
;②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为:
1:2
1:2
.(8分)现有部分短周期元素的性质或原子结构如表:
(1)用化学用语回答下列问题:
①A元素在周期表中的位置
②B元素原子结构示意图
 ;
;
③C单质分子的电子式
 ;
;
(2)元素D与元素A相比,非金属性较强的是
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去).

①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为
②若Z是红棕色气体,则Z→W的反应的化学方程式为
查看习题详情和答案>>
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子气态分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
①A元素在周期表中的位置
第三周期ⅥA族
第三周期ⅥA族
;②B元素原子结构示意图


③C单质分子的电子式


(2)元素D与元素A相比,非金属性较强的是
Cl
Cl
(用元素符号表示),下列表述中能证明这一事实的是bde
bde
(填选项序号).a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去).

①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为
BaSO4
BaSO4
;②若Z是红棕色气体,则Z→W的反应的化学方程式为
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
.A、D、E、M、L是原子序数依次增大的五种短周期元素.已知A是元素周期表中原子半径最小的元素;D的某种单质是天然存在的最硬物质;E是地壳中含量最多的元素;M与A位于同一主族;L与M能够形成ML型离子化合物.回答下列问题:
(1)元素D在元素周期表中的位置是
(2)L的单质与M的最高价氧化物对应水化物反应的离子方程式为
(3)25℃时,物质的量浓度相同的MEA、MADE3、MLE三种溶液,水的电离程度由大到小的顺序为
(4)设化合物甲、乙、丙分别为DA3EA、DA3EDA3、A2E.
ⅰ:已知:(1)丙(g)═丙(l)△H=-Q1 kJ?mol-1
(2)2甲(l)+3E2(g)═2DE2(g)+4丙(g)△H=-Q2 kJ?mol-1
Q1、Q2均大于0.若要使32g液态甲完全燃烧并恢复到室温,放出的热量为
ⅱ:已知:2甲(g)=乙(g)+丙(g).在某温度下,在1L密闭容器中加入甲,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
①该温度下反应的平衡常数为
②10min内平均反应速率v(甲)=
ⅲ:如图是乙为燃料的绿色电源工作原理示意图.若b电极的反应式为:3O2+12e-+12H+═6H2O,则a电极的反应式为:

查看习题详情和答案>>
(1)元素D在元素周期表中的位置是
第二周期第IVA族
第二周期第IVA族
.(2)L的单质与M的最高价氧化物对应水化物反应的离子方程式为
Cl2+2OH-=ClO-+Cl-+H2O
Cl2+2OH-=ClO-+Cl-+H2O
.(3)25℃时,物质的量浓度相同的MEA、MADE3、MLE三种溶液,水的电离程度由大到小的顺序为
NaClO>NaHCO3>NaOH
NaClO>NaHCO3>NaOH
.(填化学式)(4)设化合物甲、乙、丙分别为DA3EA、DA3EDA3、A2E.
ⅰ:已知:(1)丙(g)═丙(l)△H=-Q1 kJ?mol-1
(2)2甲(l)+3E2(g)═2DE2(g)+4丙(g)△H=-Q2 kJ?mol-1
Q1、Q2均大于0.若要使32g液态甲完全燃烧并恢复到室温,放出的热量为
(2Q1+0.5Q2)kJ
(2Q1+0.5Q2)kJ
.ⅱ:已知:2甲(g)=乙(g)+丙(g).在某温度下,在1L密闭容器中加入甲,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
| 物 质 | 甲 | 乙 | 丙 |
| 浓度/mol?L-1 | 0.01 | 0.2 | 0.2 |
400
400
.②10min内平均反应速率v(甲)=
0.04mol?L-1?min-1
0.04mol?L-1?min-1
.ⅲ:如图是乙为燃料的绿色电源工作原理示意图.若b电极的反应式为:3O2+12e-+12H+═6H2O,则a电极的反应式为:
(CH3)2O-12e-+3H2O=2CO2+12H+
(CH3)2O-12e-+3H2O=2CO2+12H+
.
 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,E是过渡元素且为地壳中含量较多的金属元素之一.请回答下列问题:
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,E是过渡元素且为地壳中含量较多的金属元素之一.请回答下列问题:(1)化合物M的结构简式为
HCHO
HCHO
.(2)在元素周期表中,E元素位于第
四
四
周期Ⅷ
Ⅷ
族.用电子排布式写出E元素基态原子的价电子构型3d64s2
3d64s2
.(3)元素C与D的第一电离能的大小关系是C
>
>
D(填“>”、“<”或“=”).(4)在一密闭容器中发生反应2CD2(g)?2CD(g)+D2(g)△H>O,反应过程中CD2的浓度随时间变化的情况如图所示.
①依曲线A,反应在3min内D2的平均反应速率为
0.0117mol/(L?min)
0.0117mol/(L?min)
.②若曲线A、B分别表示该反应在某不同条件下的反应情况,则此条件是
温度
温度
(填“浓度”、“压强”、“温度”或“催化剂”).③曲线A、B分别对应的反应平衡常数大小关系是KA
<
<
KB(填“>”、“<”或“=”)(5)甲同学用图1所示装置对E元素单质与浓硫酸的反应进行实验.①检查装置气密性后,将过量的E元素单质和一定量的浓硫酸放入烧瓶,塞紧橡皮塞,开始计时.t1时开始加热,在铁屑表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变.甲同学将收集到的气体体积与时间的关系粗略地表示为图2.在0~t1时间段,E表面没有气泡生成,说明E在浓硫酸中发生了
钝化
钝化
;t1~t2时间段,反应生成的气体是SO2、H2
SO2、H2
.写出开始加热时发生反应的化学方程式2Fe+6H2SO4(浓)
Fe2(SO4)3+3SO2↑+6H2O
| ||
2Fe+6H2SO4(浓)
Fe2(SO4)3+3SO2↑+6H2O
.
| ||

A、D、E、M、L是原子序数依次增大的五种短周期元素.已知A是元素周期表中原子半径最小的元素;D的某种单质是天然存在的最硬物质;E是地壳中含量最多的元素;M与A位于同一主族;L与M能够形成ML型离子化合物.回答下列问题:
(1)元素D在元素周期表中的位置是______.
(2)L的单质与M的最高价氧化物对应水化物反应的离子方程式为______.
(3)25℃时,物质的量浓度相同的MEA、MADE3、MLE三种溶液,水的电离程度由大到小的顺序为______.(填化学式)
(4)设化合物甲、乙、丙分别为DA3EA、DA3EDA3、A2E.
ⅰ:已知:(1)丙(g)═丙(l)△H=-Q1 kJ?mol-1
(2)2甲(l)+3E2(g)═2DE2(g)+4丙(g)△H=-Q2 kJ?mol-1
Q1、Q2均大于0.若要使32g液态甲完全燃烧并恢复到室温,放出的热量为______.
ⅱ:已知:2甲(g)=乙(g)+丙(g).在某温度下,在1L密闭容器中加入甲,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
①该温度下反应的平衡常数为______.
②10min内平均反应速率v(甲)=______.
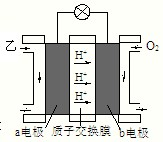
ⅲ:如图是乙为燃料的绿色电源工作原理示意图.若b电极的反应式为:3O2+12e-+12H+═6H2O,则a电极的反应式为:______.
查看习题详情和答案>>
(1)元素D在元素周期表中的位置是______.
(2)L的单质与M的最高价氧化物对应水化物反应的离子方程式为______.
(3)25℃时,物质的量浓度相同的MEA、MADE3、MLE三种溶液,水的电离程度由大到小的顺序为______.(填化学式)
(4)设化合物甲、乙、丙分别为DA3EA、DA3EDA3、A2E.
ⅰ:已知:(1)丙(g)═丙(l)△H=-Q1 kJ?mol-1
(2)2甲(l)+3E2(g)═2DE2(g)+4丙(g)△H=-Q2 kJ?mol-1
Q1、Q2均大于0.若要使32g液态甲完全燃烧并恢复到室温,放出的热量为______.
ⅱ:已知:2甲(g)=乙(g)+丙(g).在某温度下,在1L密闭容器中加入甲,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
| 物 质 | 甲 | 乙 | 丙 |
| 浓度/mol?L-1 | 0.01 | 0.2 | 0.2 |
②10min内平均反应速率v(甲)=______.
ⅲ:如图是乙为燃料的绿色电源工作原理示意图.若b电极的反应式为:3O2+12e-+12H+═6H2O,则a电极的反应式为:______.
