摘要:19.常温下.将一定量CO2通入NaOH溶液中.二者恰好完全反应.得到只含一种溶质A的溶液A的溶液.且.向该溶液中加入BaCl2溶液.生成白色沉定B.B不可用作钡餐.若误用了B.可用5%的钠盐溶液C处理.请回答: ①用离子方程式表示A溶液的原因 . ②用离子方程式表示B不可用作钡餐的原因 . ③用离子方程式表示出误用B后可用C处理的原因 . (2)在2L的密闭容器中.把3molA和4molB混合.在一定温度下发生反应: 该反应2min后达到化学平衡.生成2molC.A的体积分数为w%. 回答下列问题: ①2min内A的化学反应速率为 . ②此条件下该反应的化学平衡常为 .B的转变率为 . ③若在相同条件下向该容器中充入amolA.bmolB.cmolC.dmolD.某时刻达到平衡.A的体积分数仍为w%.则a与c满足的关系为 .
网址:http://m.1010jiajiao.com/timu_id_1720810[举报]
(1)常温下,将一定量CO2通入NaOH溶液中,二者恰好完全反应,得到只含一种溶质A的溶液A的溶液,且pH>7,向该溶液中加入BaCl2溶液,生成白色沉定B。B不可用作钡餐,若误用了B,可用5%的钠盐溶液C处理。请回答:
①用离子方程式表示A溶液pH>7的原因 。
②用离子方程式表示B不可用作钡餐的原因 。
③用离子方程式表示出误用B后可用C处理的原因 。
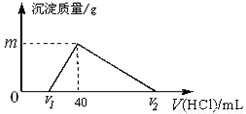
查看习题详情和答案>>常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mLpH=14的溶液,然后用1mol·L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是

A.原合金质量为0.92g
B.产生氢气的体积为896mL(标准状况下)
C.图中m的值为1.56
D.图中V2为60
查看习题详情和答案>>
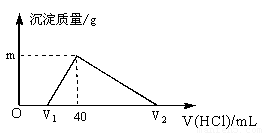
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是[来源:ZX
 XK]
XK]
A.原合金质量为0.92g[来源:Zxxk.Com]
B.产生氢气的体积为896mL(标准状况下)
C.图中m的值为1.56
D.图中V2为60
查看习题详情和答案>>